题目内容
10.能造成酸雨的气体是( )| A. | 二氧化碳 | B. | 一氧化碳 | C. | 氮气 | D. | 二氧化硫 |
分析 正常雨水的pH约为5.6,酸雨是指溶液pH小于5.6的雨水;酸雨主要由化石燃料燃烧产生的二氧化硫、氮氧化物等酸性气体,经过复杂的大气化学反应,被雨水吸收溶解而成,据此分析判断即可.
解答 解:
A、形成酸雨的主要气体是二氧化硫、二氧化氮,故选项错误.
B、形成酸雨的主要气体是二氧化硫、二氧化氮,不是CO2,故选项错误.
C、形成酸雨的主要气体是二氧化硫、二氧化氮,不是一氧化碳,故选项错误.
D、形成酸雨的主要气体是二氧化硫、二氧化氮,不是氮气,故选项正确.
故选:D.
点评 本题难度不大,酸雨是工业发展出现的副产物,了解酸雨的形成原因、危害、防治措施等是正确解答此类题的关键.

练习册系列答案
 华东师大版一课一练系列答案
华东师大版一课一练系列答案 孟建平名校考卷系列答案
孟建平名校考卷系列答案
相关题目
1.鉴别物质的方法错误的是( )
| A. | 用二氧化锰鉴别水和过氧化氢溶液 | |
| B. | 用石蕊试液鉴别一氧化碳和二氧化碳 | |
| C. | 用氯化钡溶液鉴别稀盐酸和稀硫酸 | |
| D. | 用酚酞试液鉴别食盐水和稀醋酸 |
18.生产、生活中的下列做法正确的是( )
| A. | 在室内放一盆水可以防止一氧化碳中毒 | |
| B. | 发现天然气泄漏,立即开启抽油烟机 | |
| C. | 用肥皂水区分硬水和软水 | |
| D. | 向刚刚用熟石灰改良过的酸性土壤中施用铵态氮肥 |
15.下列物质中,能和稀盐酸发生中和反应的是( )
| A. | Zn | B. | NaOH | C. | Fe2O3 | D. | CaCO3 |
18.下列说法正确的是( )
| A. | 发霉的大米煮熟后可以食用 | |
| B. | 聚氯乙烯薄膜用于食品包装 | |
| C. | 衣料中的棉和涤纶属于合成有机高分子材料 | |
| D. | 废弃塑料随意丢弃会导致白色污染 |
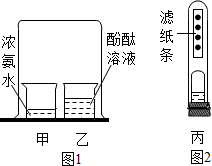 某同学对教材中探究分子性质的实验(图1)进行了改进,如图2所示,试管丙中有一张每隔1厘米滴有一滴酚酞溶液的滤纸条,装有适量浓氨水的敞口小药瓶固定在橡皮塞上. 关于图1、图2中的实验有以下说法,其中错误的是( )
某同学对教材中探究分子性质的实验(图1)进行了改进,如图2所示,试管丙中有一张每隔1厘米滴有一滴酚酞溶液的滤纸条,装有适量浓氨水的敞口小药瓶固定在橡皮塞上. 关于图1、图2中的实验有以下说法,其中错误的是( )