题目内容
12. 将一定质量的金属锌投入到98g稀硫酸中,恰好完全反应,所加稀硫酸与生成气体的质量关系如图所示,请你据此分析计算:
将一定质量的金属锌投入到98g稀硫酸中,恰好完全反应,所加稀硫酸与生成气体的质量关系如图所示,请你据此分析计算:(1)加入锌的质量6.5g.
(2)稀硫酸溶液中溶质的质量分数.
(3)反应结束后所得溶液的质量.
分析 锌和稀硫酸反应生成硫酸锌和氢气,有图中信息可知生成氢气质量是0.2g,根据氢气质量可以计算锌的质量、硫酸的质量,进一步可以计算稀硫酸溶液中溶质的质量分数和反应结束后所得溶液的质量.
解答 解:(1)设加入锌的质量为x,98g稀硫酸中硫酸质量为y,
Zn+H2SO4═ZnSO4+H2↑,
65 98 2
x y 0.2g
$\frac{65}{x}$=$\frac{98}{y}$=$\frac{2}{0.2g}$,
x=6.5g,y=9.8g,
故填:6.5.
(2)稀硫酸溶液中溶质的质量分数为:$\frac{9.8g}{98g}$×100%=10%,
答:稀硫酸溶液中溶质的质量分数为10%.
(3)反应结束后所得溶液的质量为:6.5g+98g-0.2g=104.3g,
答:反应结束后所得溶液的质量为104.3g.
点评 本题主要考查学生运用假设法和化学方程式进行计算和推断的能力,计算时要注意规范性和准确性.

练习册系列答案
相关题目
2.下列事实的解释或结论中不正确的是( )
| A. | 金属很难被压缩--是因为金属原子间间隔较小 | |
| B. | 水银温度计受热时水银柱上升--说明汞原子体积变大 | |
| C. | 煤球制成蜂窝煤后燃烧得更旺--是因为增大了煤与空气的接触面积 | |
| D. | 氢气燃烧后的生成物只有水--说明氢气是一种清洁燃料 |
20.化学兴趣小组的同学结伴到郊外河畔钓鱼,当他们看到河水浑浊并有异味时非常痛心,他们想用所学的化学知识对河水的水质进行初步探究.
(1)取回水样,在实验室里用过滤的方法将河水变的清澈.
(2)若要测定水样的酸碱度,最适宜选用的是C(填字母序号).
A.紫色石蕊试液 B.无色酚酞溶液 C.pH试纸
(3)他们检测出河水的pH为5,猜想到可能是工厂排放的酸性废水污染了河水,大家经过讨论,想到了要将工厂的酸性废水在不使用指示剂的情况下处理成中性,从下列物质中选择B(填字母序号)最好.
A.废铁 B.石灰石 C.熟石灰 D.生石灰
(4)我们通常把含有较多可溶性钙、镁化合物的水叫硬水,可以用肥皂水来鉴别硬水和软水.
(5)在活动中,某同学不小心被马蜂叮了一下(马蜂的毒液呈酸性),痛痒难耐,用下列物质涂抹可以减轻痛痒的是C(填字母序号).
A.柠檬 B.糖水 C.牙膏 D.牛奶.
(1)取回水样,在实验室里用过滤的方法将河水变的清澈.
(2)若要测定水样的酸碱度,最适宜选用的是C(填字母序号).
A.紫色石蕊试液 B.无色酚酞溶液 C.pH试纸
(3)他们检测出河水的pH为5,猜想到可能是工厂排放的酸性废水污染了河水,大家经过讨论,想到了要将工厂的酸性废水在不使用指示剂的情况下处理成中性,从下列物质中选择B(填字母序号)最好.
A.废铁 B.石灰石 C.熟石灰 D.生石灰
(4)我们通常把含有较多可溶性钙、镁化合物的水叫硬水,可以用肥皂水来鉴别硬水和软水.
(5)在活动中,某同学不小心被马蜂叮了一下(马蜂的毒液呈酸性),痛痒难耐,用下列物质涂抹可以减轻痛痒的是C(填字母序号).
| 柠檬 | 糖水 | 牙膏 | 牛奶 | |
| pH | 2~3 | 7 | 8~9 | 6~7 |
4.下列物质提纯或除杂所用试剂和分离方法正确的是( )
| 物质(括号内为杂质) | 除杂试剂 | 分离方法 | |
| A | CuO(Cu) | HCl溶液 | 溶解、过滤 |
| B | NaCl(Na2SO4) | BaCl2适量 | 吸附 |
| C | KCl(MnO2) | H2O | 溶解、过滤、蒸发、结晶 |
| D | SO2(HCl ) | NaOH | 洗气 |
| A. | A | B. | B | C. | C | D. | D |
1.分离、除杂和检验是化学实验的重要环节,下列说法不正确的是( )
| A. | 分离CO2、CO混合物时,先用NaOH溶液吸收掉CO2,分离出CO,再向该溶液加足量稀盐酸“释放”出CO2 | |
| B. | 只用一种试剂无法把稀盐酸、BaCl2溶液和KNO3溶液三种溶液区别开 | |
| C. | 要除去CaCl2溶液中混有少量稀盐酸可加入过量的CaCO3充分反应后过滤 | |
| D. | 只用组内溶液相互混合的方法就能将KOH、Na2SO4、CuSO4、MgCl2鉴别出来 |
2.下列四个图象能正确反映其对应实验操作的是( )
| A. | 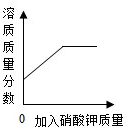 某温度下,向一定量饱和硝酸钾溶液中加入硝酸钾晶体 | |
| B. | 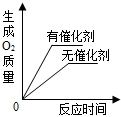 用等质量、等浓度的双氧水分别制取氧气 | |
| C. | 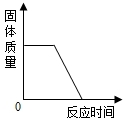 高温煅烧一定质量的石灰石 | |
| D. | 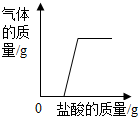 向一定量纯碱和烧碱溶液中滴入盐酸 |