题目内容
2.某粒子的结构示意图如图1所示,则(1)该粒子有三个电子层,X的值为17.
(2)该粒子的化学性质与图2C(填序号)元素的化学性质最相似.

分析 (1)根据原子结构示意图的意义分析,圆圈内的数字X表示核内质子数;原子中质子数=核外电子数;(2)根据元素的化学性质与最外层电子数关系密切进行解答.
解答 解:(1)由某元素原子结构示意图可知,有3个电子层,圆圈内的数字X表示核内质子数;原子中质子数=核外电子数,所以X=2+8+7=17;故填:3;17;
(2)元素的化学性质与最外层电子数关系密切,图1和C的最外层电子数都是7,所以化学性质相似;故填:C.
点评 本题难度不大,考查学生对粒子结构示意图及其意义的理解,明确粒子中核内质子数和核外电子数之间的关系是解题的关键.

练习册系列答案
相关题目
17.如图实验操作错误的是( )
| A. | 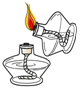 | B. | 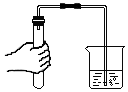 | C. | 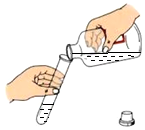 | D. | 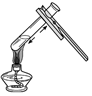 |
11.氮化镁是一种应用范围非常广泛的无机化合物,它可用于制备高硬度、高热导、抗腐蚀、抗磨损和耐高温的其它元素的氮化物,制备特殊的陶瓷材料等.某兴趣小组用镁与氮气反应制备氮化镁(Mg3N2),并用实验方法测定氮化镁的纯度.
【制备氮化镁】制备氮化镁的装备示意图如图1:
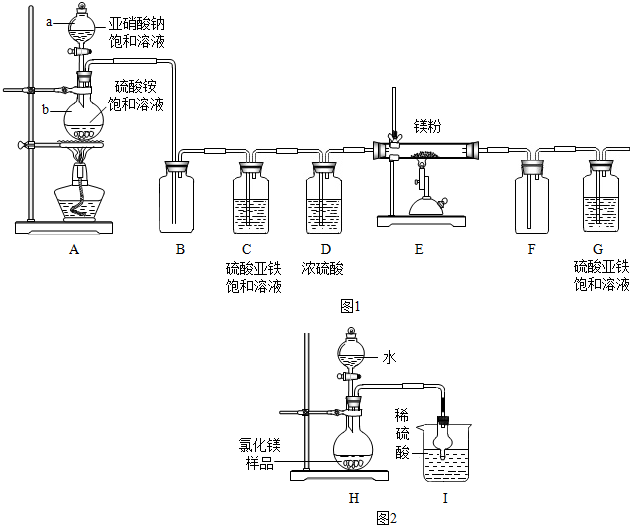
(1)仪器a的名称是分液漏斗,b的名称是圆底烧瓶;
(2)D装置的作用是吸收水蒸气(干燥氮气),G装置的作用是防止空气中的氧气进入E装置;能否将C、D装置对调否(填“能”或“否”);
(3)写出E装置中发生反应的化学方程式3Mg+N2$\frac{\underline{\;点燃\;}}{\;}$Mg3N2;
(4)检查整套装置气密性的方法是用酒精灯微热烧瓶,若G处导管口有气泡产生,且冷却后G处长导管内产生稳定的水柱,则气密性良好;
(5)进行实验时先进行A(选择“A”或“E”)处加热,理由是排尽空气;
(6)A处加热片刻后,应移去酒精灯,理由是该反应放出大量热(节约能源).
【测定氮化镁的含量】
(7)定性测定:
步骤一、取少量氮化镁样品于试管中,加足量蒸馏水,试管底部有沉淀生成,试管口闻到有刺激性气味的气体生成;
步骤二、弃去上层清液,加入稀盐酸,观察到沉淀全溶且冒气泡.
①检验刺激性气味气体的方法是将湿润的红色石蕊试纸放在试管口,若试纸变蓝,则为氨气;
②写步骤二中产生气泡的反应的化学方程式:Mg+2HCl═MgCl2+H2↑;
(8)定量测定:按如图2装置进行实验.
①球形干燥管的作用是充分反应,防倒吸;
②取氮化镁样品16克进行实验,I装置增重3.4克,求该样品中氮化镁的质量分数;62.5%
③导致该样品中氮化镁含量测定结果偏低的可能原因是产生的氨气未能全部被吸收.
| 资料一:氮化镁是浅黄色粉末,极易与水反应生成氢氧化镁沉淀和氨气; 资料二:(NH4)2SO4+2NaNO2$\frac{\underline{\;加热\;}}{\;}$2N2↑+Na2SO4+4H2O,该反应为放热反应; 资料三:饱和硫酸亚铁溶液能吸收部分氧气; 资料四:在常温下或温度不高的条件下镁几乎与水不反应. |

(1)仪器a的名称是分液漏斗,b的名称是圆底烧瓶;
(2)D装置的作用是吸收水蒸气(干燥氮气),G装置的作用是防止空气中的氧气进入E装置;能否将C、D装置对调否(填“能”或“否”);
(3)写出E装置中发生反应的化学方程式3Mg+N2$\frac{\underline{\;点燃\;}}{\;}$Mg3N2;
(4)检查整套装置气密性的方法是用酒精灯微热烧瓶,若G处导管口有气泡产生,且冷却后G处长导管内产生稳定的水柱,则气密性良好;
(5)进行实验时先进行A(选择“A”或“E”)处加热,理由是排尽空气;
(6)A处加热片刻后,应移去酒精灯,理由是该反应放出大量热(节约能源).
【测定氮化镁的含量】
(7)定性测定:
步骤一、取少量氮化镁样品于试管中,加足量蒸馏水,试管底部有沉淀生成,试管口闻到有刺激性气味的气体生成;
步骤二、弃去上层清液,加入稀盐酸,观察到沉淀全溶且冒气泡.
①检验刺激性气味气体的方法是将湿润的红色石蕊试纸放在试管口,若试纸变蓝,则为氨气;
②写步骤二中产生气泡的反应的化学方程式:Mg+2HCl═MgCl2+H2↑;
(8)定量测定:按如图2装置进行实验.
①球形干燥管的作用是充分反应,防倒吸;
②取氮化镁样品16克进行实验,I装置增重3.4克,求该样品中氮化镁的质量分数;62.5%
③导致该样品中氮化镁含量测定结果偏低的可能原因是产生的氨气未能全部被吸收.
 实验室常用如图所示装置测定空气中氧气含量.
实验室常用如图所示装置测定空气中氧气含量.