题目内容
11.几位同学根据下列各实验装置图,设计和讨论了以下问题:问题:

(1)万超同学说:“选择A与G组合成装置并在试管口加一团棉花可制取干燥氧气,其反应的化学方程式为2KMnO4$\frac{\underline{\;\;△\;\;}}{\;}$K2MnO4+MnO2+O2↑.
(2)周琦同学说:”B可用于实验室制取二氧化碳的发生装置,但应先检查装置的气密性,方法是:在导管口夹一个弹簧夹,再往长颈漏斗中加入一定量的水,漏斗内形成一段水柱,片刻后,长颈漏斗内液面不下降;,说明该装置气密性良好.“
(3)文渊同学说:“D装置装满水后可以收集并储存氧气,需要氧气时可用水将装置中的氧气排出,水应从a端(填a或b)通入.”
(4)东升同学说:“我看到课外资料上介绍,实验室可用块状硫化亚铁(FeS)与稀硫酸反应制取硫化氢气体(H2S).硫化氢气体的密度比空气大,能溶于水形成氢硫酸.根据以上知识,我现在明白了:实验室制取硫化氢气体应选用的发生装置是B,收集装置是G.”
分析 (1)根据高锰酸钾制取氧气的反应物是固体,反应条件是加热,高锰酸钾在加热的条件下生成锰酸钾、二氧化锰和氧气进行分析;
(2)根据实验室制取CO2,是在常温下,用碳酸钙和盐酸互相交换成分生成氯化钙和水和二氧化碳,因此不需要加热.二氧化碳能溶于水,密度比空气的密度大,因此只能用向上排空气法收集.实验室是用锌粒和稀硫酸在常温下反应制氢气的,氢气难溶于水,密度比空气的密度小,因此可以用排水法和向下排空气法收集.B可用于实验室制取二氧化碳(或氧气或氢气);检查装置的气密性的方法是:关闭止气夹,向长颈漏斗内加水,直到长颈漏斗内形成一段水柱,过一会儿观察水柱液面的变化,如果不下降证明严密进行分析;
(3)根据D装置装满水后可以收集并储存氧气,需要氧气时可用水将装置中的氧气排出,水应从长管进入,因为氧气的密度比水小进行分析;
(4)根据实验室制取硫化氢的反应物是固体和液体,反应条件是常温,硫化氢气体的密度比空气大,能溶于水形成氢硫酸进行分析.
解答 解:(1)高锰酸钾制取氧气的反应物是固体,反应条件是加热,高锰酸钾在加热的条件下生成锰酸钾、二氧化锰和氧气进行分析,所以选择A与G组合成装置并在试管口加一团棉花可制取干燥氧气,化学方程式为:G;2KMnO4$\frac{\underline{\;\;△\;\;}}{\;}$K2MnO4+MnO2+O2↑;
(2)二氧化碳能溶于水,密度比空气的密度大,因此只能用向上排空气法收集.实验室是用锌粒和稀硫酸在常温下反应制氢气的,氢气难溶于水,密度比空气的密度小,因此可以用排水法和向下排空气法收集.B可用于实验室制取二氧化碳(或氧气或氢气);检查装置的气密性的方法是:关闭止气夹,向长颈漏斗内加水,直到长颈漏斗内形成一段水柱,过一会儿观察水柱液面的变化,如果不下降证明严密;
(3)D装置装满水后可以收集并储存氧气,需要氧气时可用水将装置中的氧气排出,水应从长管进入,因为氧气的密度比水小,故选:a;
(4)实验室制取硫化氢的反应物是固体和液体,反应条件是常温,硫化氢气体的密度比空气大,能溶于水形成氢硫酸,所以实验室制取硫化氢气体应选用的发生装置是B,收集装置是G.
故答案为:(1)G;2KMnO4$\frac{\underline{\;\;△\;\;}}{\;}$K2MnO4+MnO2+O2↑;
(2)二氧化碳;长颈漏斗内液面不下降;
(3)a;
(4)B;G.
点评 本考点主要考查了气体的制取装置和收集装置的选择,同时也考查了化学方程式书写和装置气密性的检查等,综合性比较强.气体的制取装置的选择与反应物的状态和反应的条件有关;气体的收集装置的选择与气体的密度和溶解性有关.

| A. | 胡萝卜 | B. | 牛排 | C. | 冰淇淋 | D. | 面包 |
| 事 实 | 解 释 | |
| A | 氧气用于切割金属 | 氧气有可燃性 |
| B | 洗洁精可用于除油污 | 洗洁精能溶解油污 |
| C | 打开汽水瓶盖有大量气泡冒出 | 温度升高,气体溶解度减小 |
| D | 做铁丝燃烧实验时集气瓶底部预先要装少量的水 | 防止瓶底炸裂 |
| A. | A | B. | B | C. | C | D. | D |
| A. | O3和O2混合得到的是纯净物 | |
| B. | 臭氧层能吸收紫外线 | |
| C. | 等质量的O3和O2含有的氧原子数之比是2:3 | |
| D. | O3与O2的相互转化是物理变化 |
| A. | 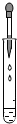 滴加液体 | B. |  闻气味 | C. | 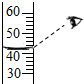 量筒读数 | D. |  熄灭酒精灯 |
| 文字表达式或化学方程式 | 相关问题 | |
| ①木炭燃烧 | 碳+氧气$\stackrel{点燃}{→}$二氧化碳或C+O2$\frac{\underline{\;点燃\;}}{\;}$CO2 | 反应基本类型是化合反应 |
| ②水的电解 | 水$\stackrel{通电}{→}$氢气+氧气或2H2O$\frac{\underline{\;通电\;}}{\;}$2H2↑+O2↑ | 反应基本类型是分解反应 |
| ③红磷在空气中燃烧 | 磷+氧气$\stackrel{点燃}{→}$五氧化二磷或4P+5O2$\frac{\underline{\;点燃\;}}{\;}$2P2O5 | 反应基本类型是化合反应 |
| ④铁丝在氧气中燃烧 | 铁+氧气$\stackrel{点燃}{→}$四氧化三铁或3Fe+2O2$\frac{\underline{\;点燃\;}}{\;}$Fe3O4 | 在做这个实验时,要事先在集气瓶中放上少量的水或细沙 |
| ⑤一种固体和一种液体反应生成一种液体和气体 | 过氧化氢$\stackrel{二氧化锰}{→}$水+氧气或2H2O2$\frac{\underline{\;MnO_2\;}}{\;}$2H2O+O2↑ | 反应基本类型是分解反应,这种固体是反应的催化剂. |
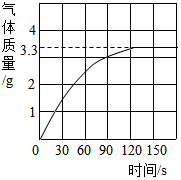 某化学兴趣小组的同学欲测定一定质量的大理石样品中碳酸钙的质量,将100g足量的稀盐酸加入到装有l0g大理石(研成粉末)的烧杯中(杂质与盐酸不反应),同时测量150s内产生的气体的质量变化,反应时间与产生气体的质量如图所示.
某化学兴趣小组的同学欲测定一定质量的大理石样品中碳酸钙的质量,将100g足量的稀盐酸加入到装有l0g大理石(研成粉末)的烧杯中(杂质与盐酸不反应),同时测量150s内产生的气体的质量变化,反应时间与产生气体的质量如图所示.