题目内容
5.CuCl常用作有机合成工业的催化剂,它是一种白色粉末,不溶于水,在空气中很容易被氧化为绿色固体Cu2(OH)3Cl.以粗盐水(含CaC12、MgC12、Na2SO4)、Cu等原料制取CuCl的工艺如下图: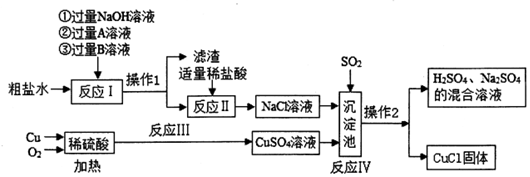
(1)CuCl的名称是氯化亚铜,操作l、操作2中用到的玻璃仪器有玻璃棒、烧杯和漏斗.
(2)反应I中,依次加入试剂①②③,若A为BaC12溶液,则B为碳酸钠溶液,加入该溶液的目的是除去氯化钙和过量的氯化钡.
(3)写出反应II中不属于中和反应的化学方程式:Na2CO3+2HCl═2NaCl+H2O+CO2↑.
(4)在工业上进行反应III时,常加入足量稀硫酸并通入过量的氧气,其目的是使铜充分反应.
(5)沉淀池中有H20参与反应,该反应Ⅳ中有2种元素的化合价发生变化.
(6)CuCl易被空气氧化的原理为:4CuCl+4H2O+O2=2Cu2(OH)3C1+2A,则A为HCl.
分析 (1)CuCl的名称是氯化亚铜,操作l、操作2都是过滤,其中用到的玻璃仪器有玻璃棒、烧杯和漏斗;
(2)氢氧化钠能和氯化镁反应生成氢氧化镁沉淀和氯化钠,氯化钡能和硫酸钠反应生成白色沉淀硫酸钡和氯化钠,碳酸钠能和氯化钙反应生成碳酸钙沉淀和氯化钠,能和氯化钡反应生成碳酸钡沉淀和氯化钠,因此加入氢氧化钠溶液可以除去氯化镁,加入氯化钡溶液可以除去硫酸钠,加入碳酸钠溶液可以除去氯化钙和过量的氯化钡;
(3)反应II中,稀盐酸和氢氧化钠反应生成氯化钠和水,和碳酸钠反应生成氯化钠、水和二氧化碳;
(4)进行反应III时,加入足量稀硫酸并通入过量的氧气,能使铜充分反应;
(5)沉淀池中有H20参与反应,该反应Ⅳ中,二氧化硫中的硫元素由+4变成+6,硫酸铜中的铜元素由+2变成+1;
(6)化学反应前后,元素种类不变,原子种类和总个数都不变.
解答 解:(1)CuCl的名称是氯化亚铜,操作l、操作2中用到的玻璃仪器有玻璃棒、烧杯和漏斗.
故填:氯化亚铜;漏斗.
(2)反应I中,依次加入试剂①②③,若A为BaC12溶液,则B为碳酸钠溶液,加入该溶液的目的是除去氯化钙和过量的氯化钡.
故填:碳酸钠;除去氯化钙和过量的氯化钡.
(3)反应II中,稀盐酸和氢氧化钠反应生成氯化钠和水,属于中和反应,和碳酸钠反应生成氯化钠、水和二氧化碳,不属于中和反应,碳酸钠和稀盐酸反应的化学方程式为:
Na2CO3+2HCl═2NaCl+H2O+CO2↑.
故填:Na2CO3+2HCl═2NaCl+H2O+CO2↑.
(4)在工业上进行反应III时,常加入足量稀硫酸并通入过量的氧气,其目的是使铜充分反应.
故填:使铜充分反应.
(5)沉淀池中有H20参与反应,该反应Ⅳ中,二氧化硫中的硫元素由+4变成+6,硫酸铜中的铜元素由+2变成+1,因此反应Ⅳ中有2种元素的化合价发生变化.
故填:2.
(6)由4CuCl+4H2O+O2=2Cu2(OH)3C1+2A可知,
反应前后铜原子都是4个,氧原子都是6个,反应前氯原子是4个,反应后应该是4个,其中2个包含在2A中,反应前氢原子是8个,反应后应该是8个,其中2个包含在2A中,则A为HCl.
故填:HCl.
点评 本题主要考查物质的性质,解答时要根据各种物质的性质,结合各方面条件进行分析、判断,从而得出正确的结论.

 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案| A. | 红磷在空气中燃烧,产生大量白雾 | |
| B. | 点燃棉花纤维能闻到烧焦的羽毛味 | |
| C. | 石灰石灼烧后变得疏松 | |
| D. | 电解水实验中,用燃着的木条检验正极端玻璃管中的气体,木条熄灭 |
| A. | 试管 | B. | 量筒 | C. | 烧杯 | D. | 锥形瓶 |
| A. | 金属材料 | B. | 合成材料 | C. | 复合材料 | D. | 天然材料 |
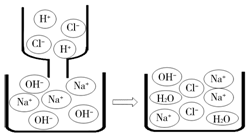
| A. | 反应前后,溶液的pH不变 | |
| B. | 向反应后溶液中滴加酚酞,溶液呈红色 | |
| C. | 该图表示氢氧化钠和盐酸恰好完全反应 | |
| D. | 该反应实质是Na+和Cl-结合生成NaCl |
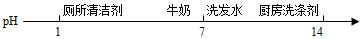
| A. | 厕所清洁剂 | B. | 牛奶 | C. | 洗发水 | D. | 厨房洗涤剂 |
| A. | 侯德榜发明侯氏联合制碱法 | |
| B. | 张青莲主持测定铟、铱等元素的相对原子质量新值 | |
| C. | 屠呦呦发现新药青蒿素 | |
| D. | 我国化学家人工合成结晶牛胰岛素 |
| A. | 含碳的化合物都是有机化合物 | |
| B. | 糖类物质不一定有甜味 | |
| C. | 糖类、油脂、蛋白质、维生素都可以为人体提供能量 | |
| D. | 淀粉、葡萄糖、纤维素、蛋白质都属于有机高分子化合物 |
| 物质 | 杂质 | 除去杂质所用的试剂和方法 | |
| A | Cu | Fe | 加入足量的稀硫酸,过滤,洗涤,干燥 |
| B | Cu(OH)2固体 | CuCl2 | 加入适量稀盐酸,过滤 |
| C | HNO3溶液 | HCl | 加适量的AgNO3溶液,过滤 |
| D | CO气体 | CO2 | 通过足量的氢氧化钠溶液,干燥 |
| A. | A | B. | B | C. | C | D. | D |