题目内容
10.为了探究某稀盐酸中溶质的质量分数,甲、乙两同学分别取溶质质量分数相等的稀盐酸100g,甲同学向其中加入氧化铜8g,反应结果后观察到固体全部消失;乙同学向其中加入氧化铜16g,反应结束后观察到固体有剩余,下列有关实验的推断正确的是( )| A. | 反应后乙同学所得溶液中一定不含盐酸 | |
| B. | 原稀盐酸中溶质的质量分数一定大于7.3%小于14.6% | |
| C. | 反应后就甲、乙两同学所得的溶液中溶质的质量分数可能相等 | |
| D. | 反应后向甲同学所得的溶液中滴加少量氢氧化钠溶液,一定会有蓝色沉淀生成 |
分析 A、反应结束,或者是盐酸反应完,或者是氧化铜反应完,或者是盐酸和氧化铜都反应完,不可能盐酸和氧化铜都有剩余.
B、甲可能恰好完全反应,也可能盐酸过量,乙盐酸一定反应完,根据此三种情况分别算出稀盐酸中溶质的质量分数.
C、若二者反应物的质量一样,则所得溶液中溶质的质量分数相等.
D、根据酸、碱、盐、氧化物之间发生反应的条件进行分析.
解答 解:A、反应结束后,固体有剩余,也就是氧化铜有剩余,那么盐酸一定反应完.故A正确;
B、甲若恰好完全反应,则稀盐酸中溶质的质量分数为7.3%,而不是大于7.3%.故B错误.
C、若8g氧化铜与100g稀盐酸恰好完全反应,则甲恰好完全反应,乙会剩余8g氧化铜,此种情况下,反应后甲、乙两同学所得的溶液中溶质的质量分数相等.故C正确;
D、氧化铜与盐酸反应生成了氯化铜,氢氧化钠与氯化铜反应会生成蓝色的氢氧化铜沉淀,而甲反应结束后氧化铜反应完,还可能有剩余的盐酸,若有剩余盐酸,盐酸又会与氢氧化铜反应生成氯化铜和水,不会出现蓝色沉淀.故D错误;
故选AC.
点评 根据本道题目中所给出的实验现象可得到多种可能,应将每种情况都分析到.

练习册系列答案
相关题目
1.“五一”节后,小红返回了学校,当她来到实验室时,意外地发现实验桌上有一瓶敞口放置的NaOH溶液,由此便激发了她的探究欲望.
【提出问题】这瓶NaOH溶液一定变质了,其变质的程度如何呢?
【猜想与假设】小红的猜想:NaOH溶液部分变质.你的不同猜想:NaOH溶液全部变质.
【收集资料】小红知道,NaOH敞口放置会变质的原因是NaOH与空气中的CO2反应,化学方程式为2NaOH+CO2=Na2CO3+H2O.
【实验探究】小红设计如下实验验证自己的猜想,请根据表中内容填写小红实验时的现象.
假设你的猜想正确,并按小红的实验方案进行实验,则你观察到的现象是产生白色沉淀;酚酞试液不变色,无明显现象.
【实验反思】保存NaOH溶液的方法是密封保存.
【提出问题】这瓶NaOH溶液一定变质了,其变质的程度如何呢?
【猜想与假设】小红的猜想:NaOH溶液部分变质.你的不同猜想:NaOH溶液全部变质.
【收集资料】小红知道,NaOH敞口放置会变质的原因是NaOH与空气中的CO2反应,化学方程式为2NaOH+CO2=Na2CO3+H2O.
【实验探究】小红设计如下实验验证自己的猜想,请根据表中内容填写小红实验时的现象.
| 实验步骤 | 现象 | 结论 |
| 第一步:取少量NaOH溶液于试管中,滴加足量的CaCl2溶液 | 产生白色沉淀 | NaOH溶液 部分变质 |
| 第二步:向上述试管中再滴加几滴酚酞试液 | 酚酞试液变红 |
【实验反思】保存NaOH溶液的方法是密封保存.
19.下列做法会损害人体健康的是( )
| A. | 用含小苏打的发酵粉焙制糕点 | B. | 用食醋除去松花蛋的涩味 | ||
| C. | 用霉变花生压榨成花生油食用 | D. | 氮气充入食品包装袋内防腐 |
20.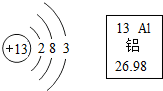 根据如图的信息判断,下列关于铝的说法正确的是( )
根据如图的信息判断,下列关于铝的说法正确的是( )
 根据如图的信息判断,下列关于铝的说法正确的是( )
根据如图的信息判断,下列关于铝的说法正确的是( )| A. | 该元素是地壳中含量最多的元素 | |
| B. | 原子的核内质子数是13 | |
| C. | 相对原子质量是26.98g | |
| D. | 在化学反应中该原子容易得到电子形成Al3+ |
 图中的A~H是初中化学常见的化合物,且分别是由H、O、S、Na、Ca、Cu中的两种或三种元索组成的.其中B、E是氧化物,E中两种元素质量之比为2:3,C、F、H为相同类别的化合物,F易溶于水并放出大量的热,G的溶液呈蓝色,图中“--”表示两端的物质间能发生化学反应;“→”表示物质间存在转化关系,部分反应物、生成物或反应条件已略去.
图中的A~H是初中化学常见的化合物,且分别是由H、O、S、Na、Ca、Cu中的两种或三种元索组成的.其中B、E是氧化物,E中两种元素质量之比为2:3,C、F、H为相同类别的化合物,F易溶于水并放出大量的热,G的溶液呈蓝色,图中“--”表示两端的物质间能发生化学反应;“→”表示物质间存在转化关系,部分反应物、生成物或反应条件已略去.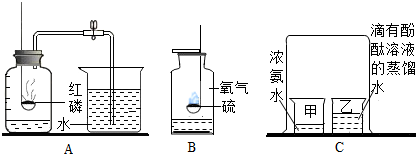
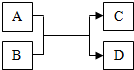 A、B、C、D都是初中化学中常见的物质,它们存在如图所示的关系(反应条件略去).
A、B、C、D都是初中化学中常见的物质,它们存在如图所示的关系(反应条件略去).