题目内容
用“>”、“<”、“=”号填在各题的方框内.
(1)钠离子的核外电子数 钠原子的核内质子数.
(2)同一化合物中正价总数的绝对值 负价总数的绝对值.
(3)电解水时生成氢气的体积 生成氧气在同状态下的体积.
(4)一个H2O分子中所含的氢原子数 一个CH4分子中所含的氢原子数.
(1)钠离子的核外电子数
(2)同一化合物中正价总数的绝对值
(3)电解水时生成氢气的体积
(4)一个H2O分子中所含的氢原子数
考点:原子和离子的相互转化,电解水实验,化合价规律和原则
专题:物质的微观构成与物质的宏观组成,空气与水
分析:根据已有的知识进行分析,钠原子失去一个电子形成钠离子;在化合物中各元素正负化合价的代数和为零;电解水生成氢气和氧气的体积比是2:1;根据分子中所含有的原子个数进行分析解答.
解答:解:A、钠原子失去一个电子形成钠离子,核外电子数是10,在原子中,核内质子数等于核外电子数是11,故钠离子和核外电子数小于钠原子的核内质子数,故填:<;
(2)在化合物中各元素正负化合价的代数和为零,故同一化合物中正价总数的绝对值等于负价总数的绝对值,故填:=;
(3)电解水生成氢气和氧气的体积比是2:1,故电解水时生成氢气的体积大于生成氧气在同状态下的体积,故填:>;
(4)一个H2O分子中所含的氢原子数是2,一个CH4分子中所含的氢原子数是4,故填:<.
(2)在化合物中各元素正负化合价的代数和为零,故同一化合物中正价总数的绝对值等于负价总数的绝对值,故填:=;
(3)电解水生成氢气和氧气的体积比是2:1,故电解水时生成氢气的体积大于生成氧气在同状态下的体积,故填:>;
(4)一个H2O分子中所含的氢原子数是2,一个CH4分子中所含的氢原子数是4,故填:<.
点评:本题考查了微粒间个数的关系,完成此题,可以依据已有的知识结合题干提供的信息进行.

练习册系列答案
 一线名师权威作业本系列答案
一线名师权威作业本系列答案
相关题目
下列几种溶液久置于空气中,溶质成分不变,但溶质的质量分数减小,且溶液质量增加的是( )
| A、浓硫酸 | B、浓盐酸 |
| C、氢氧化钠 | D、石灰水 |
下列物质中,不属于金属材料的( )
| A、钢 | B、铝 |
| C、氧化铁 | D、18K黄金 |
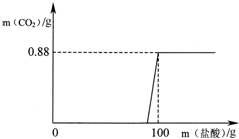 有一瓶因保存不当而部分变质的氢氧化钠固体,为测定其成分,称取10g样品配成溶液,向其中滴加溶质质量分数为7.3%的稀盐酸,放出二氧化碳气体且质量与加入稀盐酸的质量关系如右图所示.试求:样品中碳酸钠的质量是多少g?
有一瓶因保存不当而部分变质的氢氧化钠固体,为测定其成分,称取10g样品配成溶液,向其中滴加溶质质量分数为7.3%的稀盐酸,放出二氧化碳气体且质量与加入稀盐酸的质量关系如右图所示.试求:样品中碳酸钠的质量是多少g?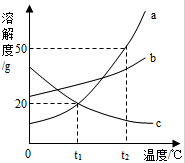 如图是三种固体物质的溶解度曲线.
如图是三种固体物质的溶解度曲线.