题目内容
3.高铁酸钾(K2FeO4)是具有紫色光泽的微细结晶粉末,它的氧化性超过高锰酸钾,是一种集氧化、吸附、凝聚、杀菌、灭菌、灭藻的新型、高效的多功能水处理剂.干燥的高铁酸钾在198℃以下是稳定的.受高热易分解为氧化铁、氧化钾与氧气,根据上述信息,请回答下列问题:(1)高铁酸钾的物理性质是紫色、结晶粉末;常温下高铁酸钾是否会分解?不会.
(2)高铁酸钾中铁元素的化合价为+6.
(3)保存高铁酸钾时应注意避免高温.
分析 (1)根据物理性质包括:颜色、状态、气味、味道、熔点、沸点、硬度、密度、导电性、导热性、延展性、溶解性、挥发性等,从题中筛选信息即可;化学性质是通过化学变化表现出来的性质.
(2)根据根据化合价原则求出元素的化合价;
(3)高铁酸钾受热时容易分解,保存时要注意防潮避热;
解答 解:(1)由题意可知,高铁酸钾是一种具有紫色光泽的微细结晶粉末属于高铁酸钾的物理性质,常温下性质稳定,不会分解.
(2)在高铁酸钾(K2FeO4)中,钾元素显+1价,氧元素显-2价,设铁元素的化合价是x,根据在化合物中正负化合价代数和为零,可得:(+1)×2+x+(-2)×4=0,则x=+6价.
(3)因为高铁酸钾受热易分解为氧化铁、某金属氧化物与氧气,所以保存高铁酸钾时应注意避免高温.
故答案为:(1)紫色、结晶粉末;(2)+6;(3)避免高温.
点评 解答本题能够正确的区分物质的物理性质和化学性质,及分析题中信息进行解题的能力,只有这样才能对问题做出正确的判断

练习册系列答案
 培优好卷单元加期末卷系列答案
培优好卷单元加期末卷系列答案
相关题目
18.下列符号能同时表示一个原子、一种元素和一种物质的是( )
| A. | O2 | B. | C | C. | H | D. | Ca2- |
13.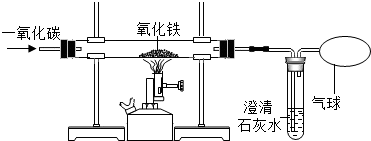 老师在课堂上演示一氧化碳还原氧化铁的实验,先通一会儿一氧化碳,以便排出装置中的空气,然后加热,反应开始后,在装置尾部用一气球收集产生的尾气,实验装置如图所示.
老师在课堂上演示一氧化碳还原氧化铁的实验,先通一会儿一氧化碳,以便排出装置中的空气,然后加热,反应开始后,在装置尾部用一气球收集产生的尾气,实验装置如图所示.
(1)请书写一氧化碳还原氧化铁的化学方程式:3CO+Fe2O3$\frac{\underline{\;高温\;}}{\;}$2Fe+3CO2.
(2)某同学只利用一瓶气体样品通过以下实验证明尾气是一氧化碳和二氧化碳的混合气体,请完成实验报告:
 老师在课堂上演示一氧化碳还原氧化铁的实验,先通一会儿一氧化碳,以便排出装置中的空气,然后加热,反应开始后,在装置尾部用一气球收集产生的尾气,实验装置如图所示.
老师在课堂上演示一氧化碳还原氧化铁的实验,先通一会儿一氧化碳,以便排出装置中的空气,然后加热,反应开始后,在装置尾部用一气球收集产生的尾气,实验装置如图所示.(1)请书写一氧化碳还原氧化铁的化学方程式:3CO+Fe2O3$\frac{\underline{\;高温\;}}{\;}$2Fe+3CO2.
(2)某同学只利用一瓶气体样品通过以下实验证明尾气是一氧化碳和二氧化碳的混合气体,请完成实验报告:
| 实验步骤 | 实验现象、结论 |
| 1、取样于集气瓶中,倒入适量澄清石灰水,振荡 | 集气瓶内的石灰水变浑浊,说明气体中含有二氧化碳 |
| 2、往步骤1中的剩余气体里伸入燃着的木条 | 集气瓶内出现蓝色火焰(放出热量)或气体燃烧,说明气体中含有一氧化碳 |
 ”“
”“ ”分别表示两种不同质子数的原子其中表示化合物的是( )
”分别表示两种不同质子数的原子其中表示化合物的是( )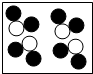

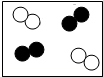
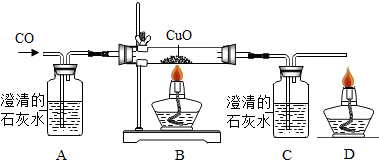 甲同学设计了如下实验装置验证一氧化碳的部分性质并验证产物.实验时,在点燃B处酒精灯之前先通入一氧化碳排出装置中的空气,然后继续实验.
甲同学设计了如下实验装置验证一氧化碳的部分性质并验证产物.实验时,在点燃B处酒精灯之前先通入一氧化碳排出装置中的空气,然后继续实验.