题目内容
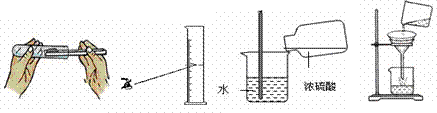
硅钢是变压器、充电器中的核心材料,其主要成份是Fe和Si。某学生用硅钢样品做了如下实验:取4.2g硅钢样品,将60g稀硫酸分6次加入样品中(其中稀硫酸与硅及其它杂质不反应),充分反应后过滤、洗涤、干燥、称重,得到的实验数据如下:
| 稀硫酸的用量 | 剩余固体的质量 |
| 第一次加入10g | mg |
| 第二次加入10g | 2.8g |
| 第三次加入10g | 2.1g |
| 第四次加入10g | 1.4g |
| 第五次加入10g | 0.7g |
| 第六次加入10g | 0.7g |
(1)从以上数据可知,稀硫酸加入第 70 次充分反应后,铁恰好完全反应。
(2)表格中m= 71 。
(3)计算所用稀硫酸中溶质的质量分数。72
70. 五(5) 71. 3.5 (每空2分)
72.[共2分,(合理解法均给分,无计算过程不给分)]
解:设所用稀硫酸中硫酸的质量分数为x,据题意得:
Fe + H2SO4 = FeSO4 + H2↑
56 98
4.2g-3.5g=0.7g 10g·x
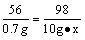 x=12.25% 答:所用稀硫酸中溶质的质量分数为12.25%。
x=12.25% 答:所用稀硫酸中溶质的质量分数为12.25%。

下列对某一主题的知识归纳,全部正确的一组是.
| A. | 水资源:废水﹣﹣﹣生活污水直接排放;硬水和软水﹣﹣﹣可用肥皂水来检验 |
| B. | 化学与健康:人体缺乏维生素B﹣﹣﹣引起坏血病;铁、锌、钙元素﹣﹣﹣都是人体必须的微量元素 |
| C. | 微观粒子:春天处处闻花香﹣﹣﹣分子在不停运动;硫离子结构示意图为: |
| D. | 食品安全:工业酒精﹣﹣﹣含有甲醇等有毒物质;不能饮用黄曲霉素(C17H12O6)﹣﹣﹣属于有机物,食用霉变后含有黄曲霉素的食物可能诱发癌变 |
向烧杯中逐滴加入X溶液至过量(图甲),生成沉淀或气体的质量(纵坐标)与加入X溶液的质量(横坐标)关系不符合图乙的是
烧杯中的物质 | X溶液 | |
A | 稀硫酸和稀盐酸 | 氯化钡溶液 |
B | 稀硫酸和硫酸铜溶液 | 氢氧化钠溶液 |
C | 澄清石灰水 | 碳酸钠溶液 |
D | 碳酸氢钠溶液 | 稀盐酸 |
20℃时,在三个各盛有100g水的容器中分别加入甲、乙、丙三种纯净物(不含结晶水,不与水反应)各10g,充分溶解后,情况如下表:
物质 | 甲 | 乙 | 丙 |
未溶解固体的质量/g | 5 | 2 | 0 |
下列说法正确的是:
A.所得溶液一定都是饱和溶液 B.丙溶液一定都是不饱和溶液
C.丙溶液溶质的质量分数最大 .D. 20℃时,甲的溶解度最大
下列属于纯净物的是( )
|
| A. | 蒸馏水 | B. | 水果色拉 | C. | 鲜奶蛋糕 | D. | 鸡汤面 |