题目内容
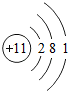
20.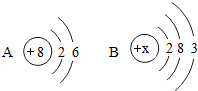 如图为A、B两种元素的原子结构示意图,请据图回答下列问题:
如图为A、B两种元素的原子结构示意图,请据图回答下列问题:①A元素单质的2个分子表示为2O2.
②B元素原子的核电荷数为13;A元素与B元素的本质区别是质子数不同.
③B元素的单质在常温下就能与A元素的单质反应生成一层致密的氧化物保护膜,请写出该反应的化学方程式4Al+3O2=2Al2O3.
分析 ①根据质子数确定元素,写出组成的单质的化学式.
②根据结构示意图的意义、元素的定义分析回答.
③根据质子数确定元素及由元素组成的单质的性质写出反应的化学方程式.
解答 解:①由元素的原子结构示意图可知,A元素为氧元素,组成的单质为氧气,2个氧分子:2O2.
②由元素的原子结构示意图可知,B元素原子的核电荷数为13;A元素与B元素的本质区别是质子数不同.
③由元素的原子结构示意图可知,B元素的单质是铝在常温下就能与A元素的单质氧气反应生成一层致密的氧化物保护膜即为氧化铝,该反应的化学方程式:4Al+3O2=2Al2O3.
故答为:①2O2;②13,质子数不同;③4Al+3O2=2Al2O3.
点评 主要考查了原子的结构示意图的意义,及元素的化学性质和元素原子的最外层电子数间的关系,培养学生的应用知识的能力.

练习册系列答案
 全能练考卷系列答案
全能练考卷系列答案
相关题目
10.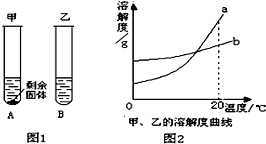 20℃时,分别向盛有10g水的两支试管中,加入等质量的甲、乙两种固体物质,使其充分溶解,可观察到如图所示的现象.
20℃时,分别向盛有10g水的两支试管中,加入等质量的甲、乙两种固体物质,使其充分溶解,可观察到如图所示的现象.
(1)20℃时,A(填“A”或“B”)试管中的溶液一定是饱和溶液;
(2)图2中表示甲物质的溶解度曲线的是b(填“a”或“b”),要使A试管中剩余的固体继续溶解可采用的方法是加水.
(3)20℃时,NaCl溶解于水的实验数据如下表.则下列叙述正确的是C.
A.②中所得溶液是饱和溶液
B.20℃时10g水最多能溶解4g NaCl
C.③④溶液的溶质质量分数相等
D.①所得溶液的溶质质量分数为20%
 20℃时,分别向盛有10g水的两支试管中,加入等质量的甲、乙两种固体物质,使其充分溶解,可观察到如图所示的现象.
20℃时,分别向盛有10g水的两支试管中,加入等质量的甲、乙两种固体物质,使其充分溶解,可观察到如图所示的现象.(1)20℃时,A(填“A”或“B”)试管中的溶液一定是饱和溶液;
(2)图2中表示甲物质的溶解度曲线的是b(填“a”或“b”),要使A试管中剩余的固体继续溶解可采用的方法是加水.
(3)20℃时,NaCl溶解于水的实验数据如下表.则下列叙述正确的是C.
| 实验序号 | 水的质量(g) | 加入NaCl的质量(g) | 溶液的质量(g) |
| ① | 10 | 2 | 12 |
| ② | 10 | 3 | 13 |
| ③ | 10 | 4 | 13.6 |
| ④ | 10 | 5 | 13.6 |
B.20℃时10g水最多能溶解4g NaCl
C.③④溶液的溶质质量分数相等
D.①所得溶液的溶质质量分数为20%
8.向Cu(NO3)2、AgNO3、Zn(NO3)2的混合溶液中加入一定质量的铁粉,充分反应后过滤,向滤出的固体中滴加稀硫酸有气泡产生,则滤出的固体物质中一定含有( )
| A. | Ag Cu Zn | B. | Ag Zn Fe | C. | Cu Zn Fe | D. | Ag Cu Fe |
15.下列几种常见的饮料中,不含有机物的可能是( )
| A. |  果汁 | B. |  牛奶 | C. |  矿泉水 | D. |  啤酒 |
5.物质的性质决定用途.下列有关说法不正确的是( )
| A. | 火碱具有碱性,故可用于改良酸性土壤 | |
| B. | 洗洁精具有乳化功能,用于去除油污 | |
| C. | 用碳素墨水写文字档案,便于长期保存 | |
| D. | 镁粉燃烧发出耀眼白光,可用于制作照明弹 |
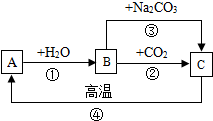 A、B、C是三种含有同一种金属元素的化合物.它们之间有如图所示的转化关系(部分产物略去).
A、B、C是三种含有同一种金属元素的化合物.它们之间有如图所示的转化关系(部分产物略去).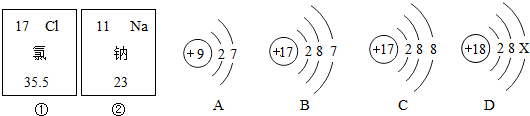
 .
.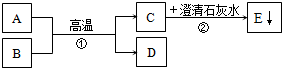 已知A为黑色固体,D为金属单质.A、B、C、D、E五种物质之间的转化关系如图所示.请回答:
已知A为黑色固体,D为金属单质.A、B、C、D、E五种物质之间的转化关系如图所示.请回答: