题目内容
18.实验室常用锌粒与稀硫酸反应制取氢气.若此过程中消耗13g锌,则制得氢气的质量是多少?分析 根据锌与硫酸反应的化学方程式,由13g锌的质量计算恰好完全反应时放出氢气的质量.
解答 解:设生成氢气的质量为x
Zn+H2SO4═ZnSO4+H2↑
65 2
13g x
$\frac{65}{13g}=\frac{2}{x}$
x=0.4g
答:制得氢气的质量是0.4g.
点评 此题是对化学方程式计算的考查,解题的关键找准相关的质量关系.

练习册系列答案
 学业测评一课一测系列答案
学业测评一课一测系列答案
相关题目
6.如图是某饮用水标签上的部分内容,下列有关说法正确的是( )


| A. | 钙可预防骨质疏松 | B. | 标签上的镁是指金属单质 | ||
| C. | 钠原子的结构示意图是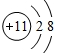 | D. | 500mL该饮用水中最多含钾5g |
3.逻辑推理是一种重要的化学思维方法,下列推理中,正确的是( )
| A. | 中和反应有水生成,有水生成的反应一定是中和反应 | |
| B. | 氧化物中一定含有氧元素,含氧元素的化合物一定是氧化物 | |
| C. | 化学变化中分子种类一定发生改变,分子种类发生改变的变化一定是化学变化 | |
| D. | 同种元素的核电荷数相同,则核电荷数相同的粒子都是同种元素 |
7.下列诗句中,不能体现分子在不断运动的是( )
| A. | 疏影横斜水清浅,暗香浮动月黄昏 | B. | 暖暖远人村,依依墟里烟 | ||
| C. | 梅须逊雪三分白,雪却输梅一段香 | D. | 有麝自来香,不用大风扬 |
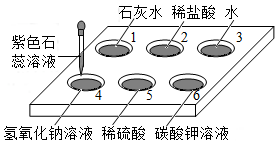 如图所示,在白色点滴板1-6的孔穴中,分别滴加2滴紫色石蕊溶液.
如图所示,在白色点滴板1-6的孔穴中,分别滴加2滴紫色石蕊溶液.