题目内容
5.采用燃烧的方法除去密闭容器中空气里的氧气,以测定空气中氧气的含量,选用下列哪种物质最为适宜( )| A. | 红磷 | B. | 硫磺 | C. | 木炭 | D. | 铁丝 |
分析 本题是考察空气成分和除杂质还有物质化学性质的一道综合题目,为整个教材除杂开始进行铺垫.题目的本意是借助氧气的化学性质,将空气中氧气除去,在除去氧气的同时要通过体积的变化体现氧气的消耗量.在选用红磷时,红磷具备了以下三点特征:(1)本身能够在空气中燃烧;(2)本身的状态为非气体;(3)生成的物质为非气态.这是本实验中选择替代物质的依据.
解答 解:A、红磷能在空气中燃烧,且生成五氧化二磷固体,故正确;
B、硫磺在空气中燃烧,但是生成物二氧化硫为气体,故错误;
C、木炭在空气中能够燃烧,生成产物为二氧化碳,当氧气浓度较低时生成物为一氧化碳,都是气体,故错误;
D、铁丝在空气中不能燃烧,故错误.
故选 A.
点评 本题对综合氧气的性质还有相关物质的性质运用进行综合考察,因此同学们在平时学习中要注意积累,同时要知识的归纳与总结.

练习册系列答案
 金博士一点全通系列答案
金博士一点全通系列答案
相关题目
15. 某实验小组欲制取氧化铜并证明氧化铜能加快氯酸钾的分解,进行了如下实验:
某实验小组欲制取氧化铜并证明氧化铜能加快氯酸钾的分解,进行了如下实验:
(一)制取氧化铜
①称取2g CuSO4•5H2O研细后倒入烧杯,加10mL蒸馏水溶解; ②向上述CuSO4溶液中逐滴加入NaOH溶液,直到不再产生沉淀,然后将所得混合物转移到蒸发皿,加热至沉淀全部变为黑色; ③将步骤②所得混合物过滤、洗涤,晾干后研细备用.回答下列问题:
(1)上述实验步骤中需要使用玻璃棒的是①②③(填实验序号),步骤①,③中研磨固体所用仪器的名称是研钵;
(2)步骤③中洗涤沉淀的操作是沿玻璃棒向漏斗中沉淀加蒸馏水至浸没沉淀,带水自然流出后,重复2-3次;
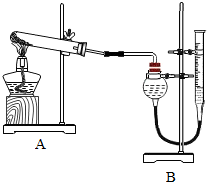
(二)证明氧化铜能加快氯酸钾的分解并与二氧化锰的催化效果进行比较用下图装置进行实验,实验时均以生成25mL气体为准,其他可能影响实验的因素均已忽略,相关数据见下表:
回答下列问题:
(3)上述实验中的“待测数据”指产生25mL气体所需时间;
(4)若要证明实验⑤中干燥管内收集的气体是O2,可待气体收集结束后,用弹簧夹夹住B中乳胶管,拔去干燥管上单孔橡皮塞,用带火星木条靠近,若木条复燃,证明收集的是氧气;
(5)为探究CuO在实验⑤中是否起催化作用,需补做如下实验(无需写出具体操作):
a.检测氧化铜反应前后质量是否改变;b.CuO的化学性质有没有改变.
 某实验小组欲制取氧化铜并证明氧化铜能加快氯酸钾的分解,进行了如下实验:
某实验小组欲制取氧化铜并证明氧化铜能加快氯酸钾的分解,进行了如下实验:(一)制取氧化铜
①称取2g CuSO4•5H2O研细后倒入烧杯,加10mL蒸馏水溶解; ②向上述CuSO4溶液中逐滴加入NaOH溶液,直到不再产生沉淀,然后将所得混合物转移到蒸发皿,加热至沉淀全部变为黑色; ③将步骤②所得混合物过滤、洗涤,晾干后研细备用.回答下列问题:
(1)上述实验步骤中需要使用玻璃棒的是①②③(填实验序号),步骤①,③中研磨固体所用仪器的名称是研钵;
(2)步骤③中洗涤沉淀的操作是沿玻璃棒向漏斗中沉淀加蒸馏水至浸没沉淀,带水自然流出后,重复2-3次;
(二)证明氧化铜能加快氯酸钾的分解并与二氧化锰的催化效果进行比较用下图装置进行实验,实验时均以生成25mL气体为准,其他可能影响实验的因素均已忽略,相关数据见下表:
| 实验序号 | KClO3质量 | 其他物质质量 | 待测数据 |
| ④ | 1.2g | 无其他物质 | |
| ⑤ | 1.2g | CuO 0.5g | |
| ⑥ | 1.2g | MnO2 0.5 |
(3)上述实验中的“待测数据”指产生25mL气体所需时间;
(4)若要证明实验⑤中干燥管内收集的气体是O2,可待气体收集结束后,用弹簧夹夹住B中乳胶管,拔去干燥管上单孔橡皮塞,用带火星木条靠近,若木条复燃,证明收集的是氧气;
(5)为探究CuO在实验⑤中是否起催化作用,需补做如下实验(无需写出具体操作):
a.检测氧化铜反应前后质量是否改变;b.CuO的化学性质有没有改变.
16.同学们用Na2CO3溶液和浓盐酸来研究简易灭火器的反应原理时,对反应后废液的成分进行探究.大家判断废液中溶质一定有NaCl(NaCl溶液呈中性),设计一个简单的实验确定废液中另一成分是Na2CO3还是盐酸.
(1)小明同学向废液中逐滴加入经硝酸酸化的AgNO3溶液来确定废液中另一成分是Na2CO3还是盐酸,小芳认为此方法不可行,原因是NaCl+AgNO3=AgCl↓+NaNO3(用化学方程式说明).
(2)小芳用实验测出废液的pH大于7,确定废液中一定含有Na2CO3.
(3)欲从废液中得到纯净的NaCl,请完成表格实验方案设计.
| 方案 | 加入试剂 | 分离方法 | 方案评价 |
| 1 | 适量Ca(NO3)2溶液 | 过滤、蒸发、结晶 | 不可行,理由是 . |
| 2 | 过量的稀盐酸 | 蒸发结晶 | 可行 |
(2)小芳用实验测出废液的pH大于7,确定废液中一定含有Na2CO3.
(3)欲从废液中得到纯净的NaCl,请完成表格实验方案设计.
13. 小王用图示的表格对所学知识进行分类归纳.其中甲包含下列关系中,不正确的一组是( )
小王用图示的表格对所学知识进行分类归纳.其中甲包含下列关系中,不正确的一组是( )
 小王用图示的表格对所学知识进行分类归纳.其中甲包含下列关系中,不正确的一组是( )
小王用图示的表格对所学知识进行分类归纳.其中甲包含下列关系中,不正确的一组是( )| 甲 | a、b、c… | |
| A | 碱 | 烧碱、纯碱、氢氧化铝 |
| B | 混合物 | 空气、盐水、石灰水 |
| C | 合金 | 不锈钢、生铁、铝合金 |
| D | 人体内的有机物 | 蛋白质、脂肪、葡萄糖 |
| A. | A | B. | B | C. | C | D. | D |
20.下列做法和对应的化学方程式均正确的是( )
| A. | 用稀盐酸除去铁制品表面的锈:2Fe+6HCl=2FeCl3+3H2↑ | |
| B. | 医疗上用氢氧化镁中和胃酸过多:Mg(OH)2+2HCl=MgCl2+H2O | |
| C. | 铝溶于稀硫酸:4Al+6H2SO4=2Al2(SO4)3+6H2↑ | |
| D. | 工业上炼铁:Fe2O3+3CO$\frac{\underline{\;高温\;}}{\;}$2Fe+3CO2 |
10.关于溶液的下列说法正确的是( )
| A. | 某溶液中有硫酸钠固体剩余,该溶液一定是硫酸钠的饱和溶液 | |
| B. | 某硫酸钠溶液中没有固体剩余,该溶液一定是硫酸钠的不饱和溶液 | |
| C. | 向某溶液中滴加硫酸钠溶液有白色固体产生,原溶液一定是硫酸钠的饱和溶液 | |
| D. | 把某硫酸钠溶液降温10℃,有晶体析出,则原溶液一定是饱和溶液 |
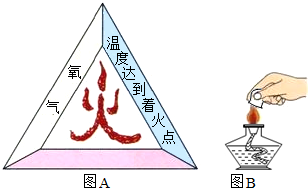 我们依据反应事实,通过比较、推理等方法可以总结归纳出灭火的规律并加以应用,请回答下列问题:
我们依据反应事实,通过比较、推理等方法可以总结归纳出灭火的规律并加以应用,请回答下列问题: