题目内容
20.有一瓶未开封的浓盐酸,部分标签如图所示.
(1)则该瓶浓盐酸的质量590g,溶质的质量是218.3g.
(2)若要配制200g溶质质量分数7.4%的稀盐酸,需要溶质质量分数 37%的浓盐酸40g,需要加入水的体积160mL.
分析 (1)根据m=ρV、溶质质量=溶液质量×溶质的质量分数,进行分析解答.
(2)根据溶液稀释前后溶质的质量不变,结合题意进行分析解答.
解答 解:(1)500mL=500cm3,m=ρV=1.18g/cm3×500cm3=590g.
溶质质量=溶液质量×溶质的质量分数,溶质的质量是590g×37%=218.3g.
(2)设需要溶质质量分数37%的浓盐酸的质量为x,根据溶液稀释前后溶质的质量不变,
则200g×7.4%=x×37% x=40g.
需要加入水的质量为200g-40g=160g(160mL).
故答案为:(1)590g;218.3;(2)40;160.
点评 本题难度不大,掌握溶质质量=溶液质量×溶质的质量分数、溶液稀释前后溶质的质量不变是正确解答本题的关键.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
5.化学实验中,人的五官起着非常重要的作用,下列五官的使用符合实验要求的是( )
| A. |  鼻子闻 | B. |  嘴巴吹 | C. |  耳朵听 | D. |  眼睛看 |

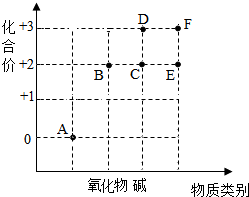 以化合价为纵坐标,以物质的类别为横坐标所绘制的图象叫价类图.如图为铁 的价类图,则 E 点可表示+2价的亚铁盐.请回答:
以化合价为纵坐标,以物质的类别为横坐标所绘制的图象叫价类图.如图为铁 的价类图,则 E 点可表示+2价的亚铁盐.请回答: