题目内容
物质X在一定温度下受热分解:2X═2N2↑+O2↑+4H2O↑ 则物质X化学式为
- A.HNO2
- B.HNO3
- C.NH3.H2O
- D.NH4NO3
分析:解此题需根据质量守恒定律,反应前后原子种类和个数都不变,分别统计出反应前后原子种类及个数,比较分析就可以求出所的物质的化学式.
解答:反应的化学方程式为2X═2N2↑+O2↑+4H2O↑,反应后反应物种含N、O、H三种元素的原子个数分别为4、6、8,根据反应前后原子种类、数目不变,可判断2X中含4个N原子、6个O原子和8个氢原子,则每个X分子由2个N原子、3个O原子和4个氢原子构成,则物质X的化学式为NH4NO3;
故选D.
点评:根据反应的化学方程式,利用反应前后原子种类、数目不变,可推断反应中某物质的分子构成、确定该物质的化学式.

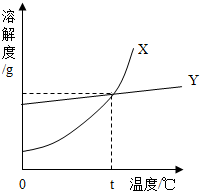 如图是X、Y两种物质的溶解度曲线,下列表述正确的是( )
如图是X、Y两种物质的溶解度曲线,下列表述正确的是( )| A、Y物质的溶解度受温度的影响较大 | B、x、Y物质的溶解度相同 | C、可用过滤的方法分离X与Y的混合物 | D、在同一温度下,X的饱和溶液一定比其不饱和溶液浓 |
下表是KNO3、NaCl在不同温度下的溶解度(单位:g/100g水)
| 温度(℃)[来源:学,科,网Z,X,X,K] | 0 | 10 | 20 | 30 | 40 | 50 | 60 | 70 | 80 | 90 | 100 |
| KNO3 | 13.3 | 20.9 | 32 | 45.8 | 64 | 85.5 | 110 | 138 | 169 | 202 | 246 |
| NaCl | 35.7 | 35.8 | 36 | 36.3 | 36.6 | 37 | 37.3 | 37.8 | 38.4 | 39 | 398 |
①以上两种物质溶解度的变化受温度影响较小的是 .
②30℃时,KNO3的溶解度是 g/100g水.
③KNO3溶液中含有少量NaCl时,可通过 的方法提纯.
④对③析出的晶体剩余溶液描述正确的是 (填写编号).
I、剩余溶液一定是KNO3饱和溶液 II、剩余溶液一定是NaCl不饱和溶液
III、上述方法可以将两者完全分开 IV、析出的晶体中只含有KNO3.
下表是KNO3 、NaCl在不同温度下的部分溶解度数据(单位:g/100g水),请回答问题:
① 10℃时,KNO3 溶解度是 (18) g/100g水。 ② 以上两种物质溶解度变化受温度影响较小的是 (19) 。 ③ 40℃时,将70gKNO3固体加入10 分搅拌,形成的溶液质量为 (20) g。 ④ 60℃时,KNO3的饱和溶液中含有少量NaCl, 通过 (21) 方法获得较纯净的KNO3晶体。 ⑤ 根据表中数据,请在坐标图中描点、绘制符合 KNO3溶解度变化规律的曲线 (22) 。 |
| ||||||||||||||||||
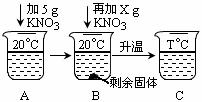
| ⑥ 向20mL水中溶解一定量KNO3固体的操作如右图: 请根据实验现象和溶解度数据回答:A、B、C中 溶液一定是饱和溶液的是 (23) ,一定是 不饱和溶液的是 (24) 。当x = (25) g 时,B中恰好没有固体剩余。 |
| ||||||||||||||||||
下表是KNO3 、NaCl在不同温度下的部分溶解度数据(单位:g/100g水),请回答问题:
① 10℃时,KNO3 溶解度是 (18) g/100g水。 ② 以上两种物质溶解度变化受温度影响较小的是 (19) 。 ③ 40℃时,将70gKNO3固体加入10 分搅拌,形成的溶液质量为 (20) g。 ④ 60℃时,KNO3的饱和溶液中含有少量NaCl, 通过 (21) 方法获得较纯净的KNO3晶体。 ⑤ 根据表中数据,请在坐标图中描点、绘制符合 KNO3溶解度变化规律的曲线 (22) 。 |
| ||||||||||||||||||
| ⑥ 向20mL水中溶解一定量KNO3固体的操作如右图: 请根据实验现象和溶解度数据回答:A、B、C中 溶液一定是饱和溶液的是 (23) ,一定是 不饱和溶液的是 (24) 。当x = (25) g 时,B中恰好没有固体剩余。 |
| ||||||||||||||||||


 0g水中,充
0g水中,充

 0g水中,充
0g水中,充