题目内容
2.酒精(C2H5OH)是常用的一种燃料.①酒精相对分子质量为46.
②酒精中碳元素和氢元素的质量比为4:1.
③184g酒精中氧元素的质量与88g二氧化碳中的氧元素质量相等.
④酒精中碳元素的质量分数为52.2%.(列式计算,结果保留0.1%)
分析 ①相对分子质量为构成分子的各原子的相对原子质量之和;
②化合物中各元素质量比=各原子的相对原子质量×原子个数之比;
③根据化合物中某元素的质量=该化合物的质量×该元素的质量分数,进行分析解答;
④根据化合物中元素质量分数的计算方法来分析.
解答 解:①酒精的相对分子质量为:12×2+1×6+16=46.故填:46;
②酒精中碳、氢元素的质量比为(12×2):(1×6)=4:1;故填:4:1;
③设酒精的质量为x,则
x×$\frac{16}{46}×100%$=88g×$\frac{16×2}{44}×100%$
x=184g
故填:184;
④酒精中碳元素的质量分数为$\frac{12×2}{46}×100%=52.2%$;故填:52.2%.
点评 本题难度不大,考查同学们灵活运用化学式的关计算进行分析问题、解决问题的能力.

练习册系列答案
 精英口算卡系列答案
精英口算卡系列答案
相关题目
12.以下对O2、CO2、SO2、MnO2四种物质组成的说法中,正确的是( )
| A. | 都含有氧元素 | B. | 都含有2个氧原子 | C. | 都含有氧分子 | D. | 都是氧化物 |
17.如图的仪器可用于实验室中盛放食盐的是( )
| A. | 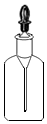 | B. | 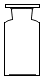 | C. | 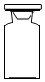 | D. | 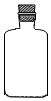 |
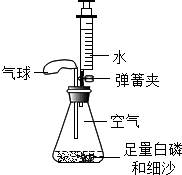 某小组利用如图装置,验证教材对空气中氧气体积分数的测量.
某小组利用如图装置,验证教材对空气中氧气体积分数的测量.