题目内容
6.利用所学化学知识解答问题:(1)已知20℃时,NaNO3的溶解度为88克,其含义是20℃时,在100克水中,溶解了88克硝酸钠便形成了饱和溶液
(2)在20℃时,将40克NaNO3溶解在50克水中,得NaNO3溶液的质量为90克,是溶液不饱和(填“饱和”或“不饱和”).若将48克NaNO3溶于50克的水中,得NaNO3溶液的质量为94克,是溶液(填“饱和”或“不饱和”)
分析 (1)固体物质的溶解度是指在一定的温度下,在100克溶剂里,该物质达到饱和状态时所能溶解的质量;
(2)在一定的温度下,在一定量的溶剂里,不能再溶解某种溶质的溶液称为饱和溶液;溶液的质量=溶质的质量+溶剂的质量.
解答 解:(1)已知20℃时,NaNO3的溶解度为88克,即20℃时,在100克水中,溶解了88克硝酸钠便形成了饱和溶液.
(2)20℃时,NaNO3的溶解度为88克,则50g水中最多溶解44g硝酸钠,将40克NaNO3溶解在50克水中,全部溶解,得NaNO3溶液的质量为:50g+40g=90g,是不饱和溶液;将48克NaNO3溶于50克的水中,只有44g溶解,得NaNO3溶液的质量为44g+50g=94g,为饱和溶液.
故答案为:(1)20℃时,在100克水中,溶解了88克硝酸钠便形成了饱和溶液;
(2)90,不饱和;94,饱和.
点评 对溶解度概念的理解要抓住四个要点:(1)条件:一定温度.(2)标准:在100克溶剂里.(3)状态:饱和.(4)单位:克.

练习册系列答案
相关题目
18.某化学兴趣小组的同学用一瓶已经过滤的澄淸透明海水为原料,在实验室中模拟“侯氏制碱法”的制碱过程.
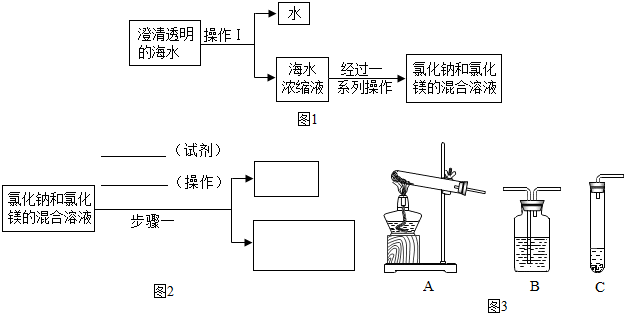
(1)从海水中分别得到纯净的水和氯化钠固体(其流程如图1),其中,操作I的名称是蒸发;完成这一操作实验,除了胶塞、导管、收集容器和铁架台外,还需要的主要仪器之一是酒精灯(只要求写出其中一种仪器名称).
(2)请完成实验设计思路图(图2),目的是从氯化钠和氯化镁的混合溶液中除去氯化镁,得到较纯净的氯化钠固体.(要求:①在图2箭头上/下方写出相应的试剂和实验操作;②在方框内写出相应的化学式;③可根据需要,仿照步骤1的写法将此图延伸.)
(3)已知有四种物质在30℃时的溶解度如表所示:
请根据溶解度表所提供的信息,用这四种物质分别作为反应物和生成物,写出一道复分解反应的化 学方程式.
NaCl+NH4HCO3=NaHCO3↓+NH4Cl.
“侯氏制碱法”既是向饱和氯化钠溶液中先后通入氨气〔NH4)和二氧化碳(CO2),使溶液中发生上述反应.
同学们利用图3装置B完成这一反应后,取其中的一种生成物,再利用装置A进行加热分解就得到了最后的产品Na2CO3(填化学式).

(1)从海水中分别得到纯净的水和氯化钠固体(其流程如图1),其中,操作I的名称是蒸发;完成这一操作实验,除了胶塞、导管、收集容器和铁架台外,还需要的主要仪器之一是酒精灯(只要求写出其中一种仪器名称).
(2)请完成实验设计思路图(图2),目的是从氯化钠和氯化镁的混合溶液中除去氯化镁,得到较纯净的氯化钠固体.(要求:①在图2箭头上/下方写出相应的试剂和实验操作;②在方框内写出相应的化学式;③可根据需要,仿照步骤1的写法将此图延伸.)
(3)已知有四种物质在30℃时的溶解度如表所示:
| 温度 | NaCl | NH4HCO3 | NaHCO3 | NH4Cl |
| 30℃ | 36.3g | 27.0g | 11.1g | 41.1g |
NaCl+NH4HCO3=NaHCO3↓+NH4Cl.
“侯氏制碱法”既是向饱和氯化钠溶液中先后通入氨气〔NH4)和二氧化碳(CO2),使溶液中发生上述反应.
同学们利用图3装置B完成这一反应后,取其中的一种生成物,再利用装置A进行加热分解就得到了最后的产品Na2CO3(填化学式).
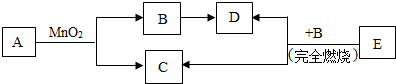 已知A、B、C、D、E五种物质之间存在以下的转化关系,其中A、C两种物质的组成元素相同,且常温下为液体.
已知A、B、C、D、E五种物质之间存在以下的转化关系,其中A、C两种物质的组成元素相同,且常温下为液体.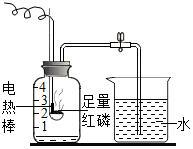 按如图组装仪器测定空气中氧气的体积分数.关闭止水夹,通电使红磷燃烧.请回答下列问题:
按如图组装仪器测定空气中氧气的体积分数.关闭止水夹,通电使红磷燃烧.请回答下列问题: