题目内容
将NH4+、NO3-、N2、NO2、NO这些粒子中,N元素表现出的化合价按从大到小的顺序排列为 .
考点:有关元素化合价的计算
专题:化学式的计算
分析:根据在化合物中正负化合价代数和为零、根中各元素的化合价的代数和为零进行分析解答本题.
解答:解:铵根显+1价,氢显+1价,根中各元素的化合价的代数和为零,设铵根中氮元素的化合价为x,则x+(+4)=+1,x=-3;
硝酸根显-1价,氧显-2价,根中各元素的化合价的代数和为零,设硝酸根中氮元素的化合价为y,则y+(-2)×3=-1,y=+5;
N2属于单质中N元素的化合价为0;
NO2中,由于氧元素显-2价,根据在化合物中正负化合价代数和为零,设N元素的化合价为z,则z+(-2)×2=0,则z=+4;
设NO中N元素的化合价为a,根据在化合物中正负化合价代数和为零,则a+(-2)=0,a=+2;
故填:NO3-、NO2、NO、N2、NH4+.
硝酸根显-1价,氧显-2价,根中各元素的化合价的代数和为零,设硝酸根中氮元素的化合价为y,则y+(-2)×3=-1,y=+5;
N2属于单质中N元素的化合价为0;
NO2中,由于氧元素显-2价,根据在化合物中正负化合价代数和为零,设N元素的化合价为z,则z+(-2)×2=0,则z=+4;
设NO中N元素的化合价为a,根据在化合物中正负化合价代数和为零,则a+(-2)=0,a=+2;
故填:NO3-、NO2、NO、N2、NH4+.
点评:本题考查学生根据在化合物中正负化合价代数和为零进行分析解题的能力.

练习册系列答案
相关题目
一辆客车夜晚行驶在公路上,发现油箱泄漏,车厢里充满了汽油味,这时应该采用的应急措施是( )
| A、洒水降温溶解汽油蒸汽 |
| B、打开所有的车窗,严禁一切烟火,疏散乘客 |
| C、让车内的乘客集中到车厢后部 |
| D、开灯查找漏油部位 |
下表列出了除去物质中少量杂质的方法,其中错误的是( )
| 选项 | 物质 | 所含杂质 | 除去杂质的方法 |
| A | CO2 | CO | 将气体点燃 |
| B | N2 | O2 | 通过灼热的铜网 |
| C | Cu | Zn | 加入过量的稀盐酸,过滤,洗涤,干燥 |
| D | FeCl2 | CuCl2 | 加入过量的铁粉,过滤 |
| A、A | B、B | C、C | D、D |
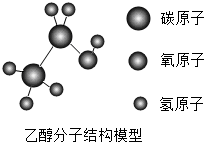 农作物的种子经过发酵、蒸馏制得的乙醇被称为“绿色汽油”.乙醇的分子结构模型如图所示,则下列叙述正确的是( )
农作物的种子经过发酵、蒸馏制得的乙醇被称为“绿色汽油”.乙醇的分子结构模型如图所示,则下列叙述正确的是( )| A、乙醇是由3种元素构成的 |
| B、一个乙醇分子中含有28个质子 |
| C、乙醇中碳、氧元素的质量比为3﹕2 |
| D、乙醇中氧元素的质量分数最大 |