题目内容
7. 如图为甲、乙两种物质(均不含结晶水)的溶解度曲线,下列说法正确的是( )
如图为甲、乙两种物质(均不含结晶水)的溶解度曲线,下列说法正确的是( )| A. | 将20℃时甲、乙两物质的饱和溶液分别升温到40℃,溶液中两物质的质量均不变 | |
| B. | 20℃时,甲、乙两种物质的溶解度均为30 | |
| C. | 乙中含有少量甲时,一般采用蒸发溶剂的方法提纯甲 | |
| D. | 40℃时,甲、乙两溶液的溶质质量分数一定不相等 |
分析 根据题目信息和溶解度曲线可知:甲、乙两种固体物质的溶解度,都是随温度升高而增大,而甲的溶解度随温度的升高变化比乙大;将20℃时甲、乙两物质的饱和溶液分别升温到40℃,溶液中两物质的质量均不变正确,都是由饱和变为不饱和溶液;20℃时,甲、乙两种物质的溶解度均为30错误,因为溶解度没有单位;乙中含有少量甲时,一般采用蒸发溶剂的方法提纯甲错误,应该是降温结晶,因为甲的溶解度随温度的升高变化比乙大;40℃时,甲、乙两溶液的溶质质量分数一定不相等错误,因为没有指明是饱和溶液.
解答 解:A、将20℃时甲、乙两物质的饱和溶液分别升温到40℃,溶液中两物质的质量均不变正确,都是由饱和变为不饱和溶液;故选项正确;
B、20℃时,甲、乙两种物质的溶解度均为30错误,因为溶解度没有单位;故选项错误;
C、乙中含有少量甲时,一般采用蒸发溶剂的方法提纯甲错误,应该是降温结晶,因为甲的溶解度随温度的升高变化比乙大;故选项错误;
D、40℃时,甲、乙两溶液的溶质质量分数一定不相等错误,因为没有指明是饱和溶液;故选项错误;
故选A
点评 本考点考查了溶解度曲线及其应用,通过溶解度曲线我们可以获得很多信息;还考查了有关溶液结晶的方法等,本考点主要出现在选择题和填空题中.

练习册系列答案
 全能练考卷系列答案
全能练考卷系列答案 一课一练课时达标系列答案
一课一练课时达标系列答案
相关题目
15.某实验小组利用废硫酸液制备K2SO4的流程如图.

(1)请补充完整反应Ⅱ的化学方程式:H2O+CaSO4+2NH3+CO2═CaCO3↓+(NH4)2SO4.
(2)上述流程中可循环使用的物质有CO2和CaCO3(填写化学式).
(3)反应Ⅲ中相关物质的溶解度如表所示.你认为反应Ⅲ在常温下能实现的原因是常温下硫酸钾溶解度最小.
(4)不用水而用饱和K2SO4溶液洗涤反应Ⅲ所得晶体的目的是防止硫酸钾溶解在水中;为检验此晶体是否洗涤干净,可取最后一次洗涤液,先加入c(选填序号,下同),振荡、静置,再向上层清液中滴加a,观察现象即可判断.
a.AgNO3溶液 b.过量的BaCl2溶液 c.过量的Ba(NO3)2溶液.

(1)请补充完整反应Ⅱ的化学方程式:H2O+CaSO4+2NH3+CO2═CaCO3↓+(NH4)2SO4.
(2)上述流程中可循环使用的物质有CO2和CaCO3(填写化学式).
(3)反应Ⅲ中相关物质的溶解度如表所示.你认为反应Ⅲ在常温下能实现的原因是常温下硫酸钾溶解度最小.
| 物质 | KCl | K2SO4 | NH4Cl | M |
| 溶解度/g(25℃) | 34.0 | 11.1 | 37.2 | 19.5 |
a.AgNO3溶液 b.过量的BaCl2溶液 c.过量的Ba(NO3)2溶液.
2.对下列事实的解释不正确的是( )
| 选项 | 事实 | 解释 |
| A | 氢氧化钾溶液显碱性 | 溶液中含有氢氧根离子 |
| B | 一氧化碳、二氧化碳性质不同 | 分子结构不同 |
| C | 酸碱盐溶液导电 | 溶液中有大量自由移动的电子 |
| D | 湿衣服晾干 | 分子不断运动 |
| A. | A | B. | B | C. | C | D. | D |
12.分类法在日常生活和科学研究中具有广泛的应用.化学实验可以按照实验目的分为:探究物理性质实验、探究物质含量实验、探究反应条件实验等.
(1)按照实验目的不同可以将D与C归为一组,分类依据是都是探究物质含量的实验.
(2)氢气能在氯气中燃烧生成氯化氢气体,镁带能在二氧化碳气体中燃烧发生置换反应生成一黑一白两种固体,请写出镁带在二氧化碳中燃烧的化学方程式2Mg+CO2$\frac{\underline{\;点燃\;}}{\;}$C+2MgO,由此可推知,氯气和二氧化碳具有和氧气相似的化学性质.
| A | B | C | D |
 |  |  |  |
| 铁钉锈蚀条件的探究 | 酸和碱与指示剂的作用 | 测定空气中氧气含量 | 取两块干燥的玻璃片,对着其中一块哈气 |
(2)氢气能在氯气中燃烧生成氯化氢气体,镁带能在二氧化碳气体中燃烧发生置换反应生成一黑一白两种固体,请写出镁带在二氧化碳中燃烧的化学方程式2Mg+CO2$\frac{\underline{\;点燃\;}}{\;}$C+2MgO,由此可推知,氯气和二氧化碳具有和氧气相似的化学性质.
19.下列各组中的物质混合,形成溶液的质量比反应前溶液的总质量减少的是( )
| A. | 铁和稀硫酸 | B. | 氢氧化钾溶液中加入稀硝酸 | ||
| C. | 硫酸铜溶液中加入锌片 | D. | 氢氧化钙溶液中加入碳酸钾溶液 |
17.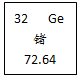 锗是重要的半导体材料.在元素周期表中,锗元素的信息如图所示,对图中信息解释不正确的是( )
锗是重要的半导体材料.在元素周期表中,锗元素的信息如图所示,对图中信息解释不正确的是( )
 锗是重要的半导体材料.在元素周期表中,锗元素的信息如图所示,对图中信息解释不正确的是( )
锗是重要的半导体材料.在元素周期表中,锗元素的信息如图所示,对图中信息解释不正确的是( )| A. | 原子序数为32 | B. | 元素名称为锗 | ||
| C. | 元素符号为Ge | D. | 相对原子质量为32 |