题目内容
10.根据下列实验装置进行有关实验,回答下列问题.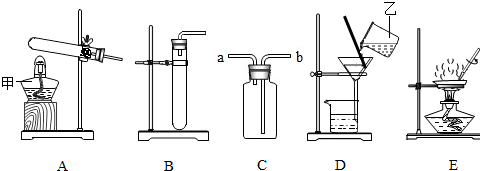
(1)写出图中指定仪器的名称:甲酒精灯,乙烧杯.
(2)实验室用高锰酸钾制取氧气,发生装置可选择图中的A(填标号),写出该反应化学方程式2KMnO4$\frac{\underline{\;\;△\;\;}}{\;}$K2MnO4+MnO2+O2↑.用充满水的装置C收集氧气,则氧气需从a(填“a”或“b”)端通入.
(3)实验室制取二氧化碳的化学方程式是CaCO3+2HCl=CaCl2+CO2↑+H2O,用装置C收集二氧化碳,验满时,燃着木条应放在a(填“a”或”b”)端口.
(4)用上述制取二氧化碳实验后的固液残留物进行过滤、蒸发的操作练习.
①对固液残留物进行过滤,选择图中D装置,过滤时玻璃捧的作用是引流;
②少量滤液进行蒸发,蒸发过程中用玻璃棒不断搅拌的目的是受热均匀,防止液滴飞溅,析出的固体中一定含有的物质是氯化钙.
分析 (1)依据常用仪器回答;
(2)依据高锰酸钾制取氧气的反应原理书写方程式;依据制取氧气的反应物的状态和反应条件选择发生装置;据氧气的密度和溶解性选择收集装置;
(3)据二氧化碳的实验室制取原理写出方程式;据二氧化碳验满的方法解答;
(4)①图示过滤装置是D,玻璃棒在实验中起引流的作用;
②大理石的主要成分碳酸钙和盐酸反应生成氯化钙,所以反应后析出固体中一定含有氯化钙
解答 解:(1)试管是常用的反应容器,故答案为:酒精灯、烧杯;
(2)高锰酸钾在加热下分解为锰酸钾、二氧化锰和氧气,方程式是2KMnO4$\frac{\underline{\;\;△\;\;}}{\;}$K2MnO4+MnO2+O2↑;反应需加热,发生装置选择A;用充满水的装置C收集氧气,氧气不易溶于水,可应用排水法收集,则氧气需从a进入;
(3)二氧化碳的实验室制法是用稀盐酸与大理石(或石灰石.其主要成分都是碳酸钙)反应来制取.其反应原理是CaCO3+2HCl=CaCl2+CO2↑+H2O;二氧化碳的密度比空气大,可用向上排空气法收集,用装置C收集二氧化碳,应长进短出,验满时,燃着木条应放在a端;
(4))①图示过滤装置是D,玻璃棒在实验中起引流的作用;
②大理石的主要成分碳酸钙和盐酸反应生成氯化钙,所以反应后析出固体中一定含有氯化钙;取上述少量滤液进行蒸发,蒸发过程中玻璃棒不断搅拌的目的是受热均匀,防止液滴飞溅.
故答案为:(1)酒精灯、烧杯;
(2)2KMnO4$\frac{\underline{\;\;△\;\;}}{\;}$K2MnO4+MnO2+O2↑、A、a;
(3)CaCO3+2HCl=CaCl2+CO2↑+H2O、a;
(4)①引流;②受热均匀,防止液滴飞溅、氯化钙.
点评 明确实验室制取氧气、二氧化碳的反应原理、收集方法,及过滤实验操作等知识,即可结合题意顺利解答

| A. | 油锅着火,泼水灭火 | |
| B. | 森林发生火灾,可砍掉部分树木,形成隔离带 | |
| C. | 堆放杂物的纸箱着火,用水浇灭 | |
| D. | 不慎碰倒酒精灯,酒精在桌面上燃烧,立即用湿抹布扑盖 |
| A. | 硬水与软水可以用肥皂水鉴别 | |
| B. | 水中溶有的有色物质可用活性炭吸附 | |
| C. | 水通电分解生成的氢气与氧气的质量比为2:1 | |
| D. | 为减少水体污染,要合理使用农药、化肥 |
 在学习了单质碳的化学性质后,我们知道反应物的用量不同,生成物可能不同,于是同学们联想到木炭与氧化铜发生的反应可能有:
在学习了单质碳的化学性质后,我们知道反应物的用量不同,生成物可能不同,于是同学们联想到木炭与氧化铜发生的反应可能有:请你喝它们一起进行探究来验证上述想法.
【查阅资料】CO能使湿润的黄色氯化钯试纸变成蓝色,二氧化碳不反应.
【猜想与假设】木炭与氧化铜反应生成的产物有三种可能:
(1)产物是:铜和一氧化碳;
(2)产物是:铜和二氧化碳;
(3)产物是:铜、一氧化碳和二氧化碳.
【设计方案】
(1)检验CO2的方法是Ca(OH)2+CO2=CaCO3↓+H2O(用化学方程式表示);
(2)检验产物中是否存在CO,同学们设计了如下实验(装置如图),请填写实验报告.
| 实 验 现 象 | 实 验 结 论 |
| ①装置A的试管中固体由黑色变为红色; ②B中黄色试纸变蓝 ③C中澄清石灰水变浑浊 | ①有铜生成 ②有一氧化碳生成 ③有二氧化碳生成 |
①实验结束时,为防止Cu被氧化,必须先停止加热,待铜冷却后再将试管口的胶塞取下,因此,若没有B安全瓶,可能导致的后果是溶液或澄清石灰水倒流到试管里使试管炸裂.
②根据实验结论,从环保角度考虑,上述装置C后应添加的装置是加尾气处理装置.
| A. | Na | B. | K | C. | I | D. | O |
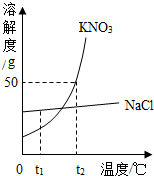 如图为硝酸钾和氯化钠两种固体物质的溶解度曲线.
如图为硝酸钾和氯化钠两种固体物质的溶解度曲线. 微观模拟题:通过如图反应示意图回答下列问题:
微观模拟题:通过如图反应示意图回答下列问题: