题目内容
17.根据下列装置图,回答有关问题: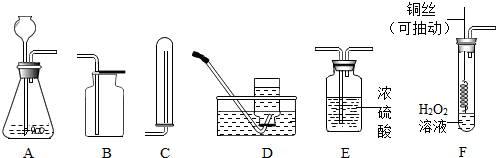
(1)实验室用过氧化氢制取氧气的化学方程式为2H2O2$\frac{\underline{\;MnO_2\;}}{\;}$2H2O+O2↑,若要制取并收集一瓶干燥的氧气,应选用装置的连接顺序为A、E、B(选填字母),检验氧气是否收集满的方法为用一根带火星的木条放在集气瓶口.
(2)实验室常用锌粒和稀硫酸反应制取氢气,有关反应的化学方程式为Zn+H2SO4=ZnSO4+H2↑.若用排空气法收集,应选用的收集装置为C(选填字母).
(3)实验改进:查阅资料发现,氧化铜可以用作过氧化氢分解制氧气的催化剂.现有一根洁净的铜丝,实验前先将其绕成螺旋状,再经过灼烧处理.改进后的发生装置如图F所示(己略去夹持装置).
①铜丝绕成螺旋状的作用是B.
A.收集到更多的02 B.加快反应速率 C.没有影响
②与装置A比较,改进后装置的优点是可随时控制反应的进行.
分析 (1)根据实验室中制取氧气的原理、干燥收集方法以及氧气的验满方法来分析;
(2)锌与稀硫酸反应生成硫酸锌和氢气,氢气的密度比空气小;
(3)铜在加热的条件下转化为氧化铜;将铜丝绕成螺旋状,增大了与氧气的接触面积;根据改进后的装置的特点来分析.
解答 解:(1)过氧化氢在二氧化锰的催化作用下分解为水和氧气;因为反应物是固体与液体,在常温下进行,选择装置A来制取,收集一瓶干燥的氧气,用浓硫酸来进行干燥,用向上排空气法来收集;氧气验满时,可将一根带火星的木条放在集气瓶口,观察木条是否复燃;故填:2H2O2$\frac{\underline{\;MnO_2\;}}{\;}$2H2O+O2↑;A、E、B;用一根带火星的木条放在集气瓶口;
(2)锌和稀硫酸反应生成硫酸锌和氢气,因为氢气的密度比空气小,所以可用向下排空气法来收集;故填:Zn+H2SO4=ZnSO4+H2↑;C;
(3)将铜丝灼烧,铜与氧气反应生成氧化铜;故填:灼烧;
①将铜丝绕成螺旋状,增大了与反应物的接触面积,加快了反应的速率;故填:B;
②改进后的装置,通过抽动铜丝来控制反应的发生和停止;故填:可随时控制反应的进行.
点评 本题考查了装置的选择、化学方程式的书写、实验装置的改进,难度不大.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
7.在一定条件下,一个密闭容器内发生某反应,测得反应前后各物质的质量如下表所示,下列有关说法不正确的是( )
| 物质 | M | N | P | Q |
| 反应前质量/g | 16 | 24 | 15 | 20 |
| 反应后质量/g | x | y | 0 | 10 |
| A. | 参加反应的P与Q的质量比为3:2 | B. | x的取值范围:0≤x≤30 | ||
| C. | 当y≤24时,该反应一定是化合反应 | D. | x+y=65 |
5.下列措施或事故处理方法不正确的是( )
| A. | 用盐酸除去铁钉表面的铁锈 | |
| B. | 用甲醛浸泡海产品防止变质 | |
| C. | 炒菜时油锅着火,立即用锅盖盖灭 | |
| D. | 氢氧化钠溶液不慎沾在皮肤上,要用大量水冲洗,再涂上硼酸溶液 |
2.下列化学用语与所表述的意义相符的是( )
①2Ca2+--2个钙离子 ②O2--2个氧原子 ③2H2O--2个水分子
④2H--2个氢元素 ⑤$\stackrel{0}{{N}_{2}}$--氮气中氮元素的化合价为零.
①2Ca2+--2个钙离子 ②O2--2个氧原子 ③2H2O--2个水分子
④2H--2个氢元素 ⑤$\stackrel{0}{{N}_{2}}$--氮气中氮元素的化合价为零.
| A. | ①④⑤ | B. | ②④ | C. | ①③⑤ | D. | ②③ |
6.下列各组物质在水中能大量共存的是( )
| A. | NaOH Na2CO3 H2SO4 | B. | NaCl Na2SO4 Na2CO3 | ||
| C. | NaCl Ba(NO3)2 K2SO4 | D. | CuSO4 Na2SO4 NaOH |
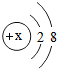 .
.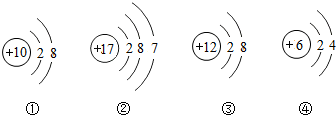
 ”表示氧原子,“
”表示氧原子,“ ”表示氢原子).
”表示氢原子).

 我县也发现了人感染H7N9禽流感病例.我们平时要养成良好的卫生习惯,勤洗手,室内勤通风换气,注意营养,保证充足的睡眠和休息,加强体育锻炼,尽量避免直接接触活禽,鸟类或其粪便.人感染H7N9禽流感是由H7N9禽流感病毒引起的急性呼吸道传染病.
我县也发现了人感染H7N9禽流感病例.我们平时要养成良好的卫生习惯,勤洗手,室内勤通风换气,注意营养,保证充足的睡眠和休息,加强体育锻炼,尽量避免直接接触活禽,鸟类或其粪便.人感染H7N9禽流感是由H7N9禽流感病毒引起的急性呼吸道传染病.