题目内容
2. 铝及铝的化合物在生产生活中有许多重要用途.
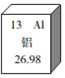
铝及铝的化合物在生产生活中有许多重要用途.(1)元素周期表中铝元素的部分信息如图所示,从中可获得的一条信息是铝原子核外电子数是13;
(2)家里的铝制饮具不宜用钢刷来擦洗,其原因是防止破坏铝制饮具的保护膜;
(3)铝合金被广泛应用于飞机制造上,作为材料,铝合金与钢铁相比,其主要优点有密度小(任答一条).
(4)明矾是一种含铝的硫酸盐,可用于净水,这是因为明矾溶于水生成的胶状物可以吸附悬浮于水中的杂质,使之从水中沉降出来;
(5)胃舒平是治疗胃酸过多的常用药物,其中含有的有效成分是氢氧化铝,其治疗原理用化学方程式表示Al(OH)3+3HCl═AlCl3+3H2O.
分析 (1)根据元素在元素周期表中的位置可以判断相关方面的问题;
(2)通常情况下,铝能和空气中的氧气反应生成氧化铝保护膜;
(3)铝合金与钢铁相比,其主要优点有密度小、耐腐蚀等;
(4)明矾溶于水生成的胶状物可以吸附悬浮于水中的杂质,使之从水中沉降出来;
(5)氢氧化铝能和胃酸中的盐酸反应生成氯化铝和水.
解答 解:(1)元素周期表中铝元素的部分信息如图所示,从中可获得的信息是铝原子核外电子数是13,核内质子数是13,原子序数是13等.
故填:铝原子核外电子数是13.
(2)家里的铝制饮具不宜用钢刷来擦洗,目的是为了防止破坏铝制饮具的保护膜.
故填:防止破坏铝制饮具的保护膜.
(3)作为材料,铝合金与钢铁相比,其主要优点有密度小、耐腐蚀等.
故填:密度小.
(4)明矾是一种含铝的硫酸盐,可用于净水,这是因为明矾溶于水生成的胶状物可以吸附悬浮于水中的杂质,使之从水中沉降出来.
故填:吸附.
(5)胃舒平治疗原理是氢氧化铝能和胃酸中的盐酸反应生成氯化铝和水,反应的化学方程式为:Al(OH)3+3HCl═AlCl3+3H2O.
故填:Al(OH)3+3HCl═AlCl3+3H2O.
点评 本题主要考查物质的性质,解答时要根据各种物质的性质,结合各方面条件进行分析、判断,从而得出正确的结论.

练习册系列答案
相关题目
12.除去CO中混有的少量CO2,下列方法中正确的是( )
| A. | 将混合气体点燃 | B. | 通入灼热的氧化铜中 | ||
| C. | 将混合气体通入稀盐酸中 | D. | 将混合气体通入澄清的石灰水中 |
7.下列叙述、对应的原理(用化学方程式表示)和基本反应类型都正确的是( )
点燃.
点燃.
| A. | 用磷做烟幕弹 4P+5O2$\frac{\underline{\;点燃\;}}{\;}$P2O5 化合反应 | |
| B. | 焦炭还原氧化铁 2Fe2O3+3C$\frac{\underline{\;高温\;}}{\;}$4Fe+3CO2 还原反应 | |
| C. | 用过氧化氢溶液制取氧气 2H2O2$\frac{\underline{\;MnO_2\;}}{\;}$2H2O+O2↑ 分解反应 | |
| D. | 用铁丝燃烧探究空气中氧气含量 3Fe+2O2═Fe3O4 化合反应 |
14.下列做法正确的是( )
| A. | 节能减排,使用含磷洗衣粉 | |
| B. | 变废为宝,焚烧秸秆并将灰烬做肥料 | |
| C. | 方便生活,推广使用一次性塑料餐盒 | |
| D. | 绿色出行,提倡乘坐公共交通工具 |
12.下列做法不科学的是( )
| A. | 用干冰人工降雨 | B. | 用熟石灰中和酸性土壤 | ||
| C. | 服用氢氧化钠治胃病 | D. | 用食醋除去水垢 |
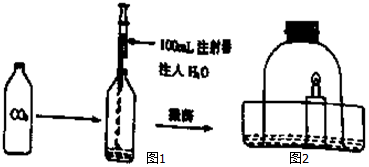
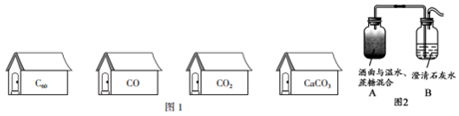





 A~L均为初中化学常见物质,其中A是大理石主要成分,B是人体胃酸的一种主要成分,E是钠盐,它们之间有如右图所示的相互转换关系(图中部分生成物已略去)请回答下列问题:
A~L均为初中化学常见物质,其中A是大理石主要成分,B是人体胃酸的一种主要成分,E是钠盐,它们之间有如右图所示的相互转换关系(图中部分生成物已略去)请回答下列问题: