题目内容
2.12.2g铁粉与铜粉的混合物,放入足量的硫酸铜溶液中,完全反应后,共得红色固体12.6g.求原混合物中铜的质量.分析 铁和硫酸铜反应生成硫酸亚铁和铜,根据反应的化学方程式和提供的数据可以计算原混合物中铜的质量.
解答 解:设原混合物中铁的质量为x,
Fe+CuSO4═FeSO4+Cu,固体增加质量
56 64 64-56=8
x 12.6g-12.2g=0.4g
$\frac{56}{x}$=$\frac{8}{0.4g}$,
x=2.8g,
原混合物中铜的质量为:12.2g-2.8g=9.4g,
答:原混合物中铜的质量是9.4g.
点评 差量法在计算中的应用很广泛,解答的关键是要分析出物质的质量差与要求的未知数之间的关系,再根据具体的数据求解.

练习册系列答案
相关题目
13.区分O2、CO、CO2三种其他最简单的方法是( )
| A. | 将气体通入澄清石灰水 | B. | 将气体通入灼热的氧化铜 | ||
| C. | 将气体通过灼热的铜网 | D. | 将燃着的木条伸入集气瓶 |
10.下列物质可以由金属与酸反应制得的是( )
| A. | 氯化铁 | B. | 氯化铜 | C. | 氯化亚铁 | D. | 氯化铝 |
17.将铁片插入下列溶液中,片刻取出,溶液的质量会减少的是( )
| A. | 盐酸 | B. | 硫酸铜 | C. | 稀硫酸 | D. | 硫酸锌 |
12.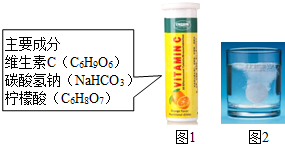 某研究小组发现,维C泡腾片(保健药品,主要成分见图1)溶于水,有许多气泡产生(如图2).该小组同学
某研究小组发现,维C泡腾片(保健药品,主要成分见图1)溶于水,有许多气泡产生(如图2).该小组同学
进行如下探究.
探究一:该气体的成分.
【猜想与假设】
小腾说:该气体可能是CO2、O2、CO、H2、N2.
小献说:不可能含有N2,因为?根据质量守恒定律(或化学反应前后元素种类不变),反应物中不含氮元素.
小伍说:不可能含有CO和H2,因为从药品安全角度考虑,不可能含有H2,因为H2易燃易爆;不可能含有CO的原因是?有毒.
最后同学一致认为:该气体可能含有CO2、O2中的一种或两种.
【进行实验】
【得出结论】
(1)由实验①可知,该气体中肯定含有二氧化碳,写出①反应的化学方程式Ca(OH)2+CO2=CaCO3↓+H2O.
你认为,生成该气体是由维C泡腾中的碳酸氢钠和柠檬酸生成的.
(2)由实验②不能(填“能”或“不能”)确定该气体中不含氧气,理由是若生成氧气和二氧化碳的混合物,当氧气含量过少时,带火星的木条也不能复燃.
探究二:维C泡腾片溶液的酸碱性.
(3)向维C泡腾片溶液中滴加石蕊试液,溶液变红,说明溶液显酸性,PH<7(填“>”、“<”、“﹦”).
 某研究小组发现,维C泡腾片(保健药品,主要成分见图1)溶于水,有许多气泡产生(如图2).该小组同学
某研究小组发现,维C泡腾片(保健药品,主要成分见图1)溶于水,有许多气泡产生(如图2).该小组同学进行如下探究.
探究一:该气体的成分.
【猜想与假设】
小腾说:该气体可能是CO2、O2、CO、H2、N2.
小献说:不可能含有N2,因为?根据质量守恒定律(或化学反应前后元素种类不变),反应物中不含氮元素.
小伍说:不可能含有CO和H2,因为从药品安全角度考虑,不可能含有H2,因为H2易燃易爆;不可能含有CO的原因是?有毒.
最后同学一致认为:该气体可能含有CO2、O2中的一种或两种.
【进行实验】
| 实验编号 | 实验操作 | 实验现象 |
| ① | 将气体通入澄清的石灰水中 | 澄清石灰水变浑浊 |
| ② | 将带火星的木条伸入该气体中 | 带火星的木条没有复燃 |
(1)由实验①可知,该气体中肯定含有二氧化碳,写出①反应的化学方程式Ca(OH)2+CO2=CaCO3↓+H2O.
你认为,生成该气体是由维C泡腾中的碳酸氢钠和柠檬酸生成的.
(2)由实验②不能(填“能”或“不能”)确定该气体中不含氧气,理由是若生成氧气和二氧化碳的混合物,当氧气含量过少时,带火星的木条也不能复燃.
探究二:维C泡腾片溶液的酸碱性.
(3)向维C泡腾片溶液中滴加石蕊试液,溶液变红,说明溶液显酸性,PH<7(填“>”、“<”、“﹦”).
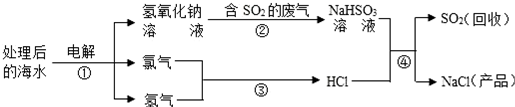

 ①当a=10时,该粒子是原子.
①当a=10时,该粒子是原子.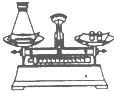 如图是测定白磷燃烧后前后质量变化和测定空气组成的实验,已知白磷燃烧的现象和产物与红磷燃烧相同,试回答下列问题:
如图是测定白磷燃烧后前后质量变化和测定空气组成的实验,已知白磷燃烧的现象和产物与红磷燃烧相同,试回答下列问题: