题目内容
中和反应在工农业和生活中有广泛的应用.某学生课外兴趣小组对中和反应进行研究.
(1)对于没有明显实验现象产生的中和反应,如稀盐酸与稀氢氧化钠溶液的反应,要证明它们之间确实发生了化学反应,可通过如下实验来进行.
①在盛有稀氢氧化钠溶液的烧杯中,滴加2~3滴酚酞试液,用胶头滴管吸取稀盐酸逐滴加入到上述烧杯中,边滴边用玻璃棒搅拌,当观察到 现象时,说明它们之间发生了中和反应,且恰好完全反应.
②将稀盐酸逐滴匀速加入一定量的稀氢氧化钠溶液中,用数字化仪器对反应过程中溶液的温度、PH进行实时测定,得到的曲线如图1、图12所示.
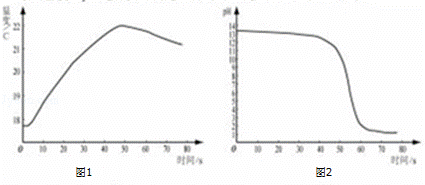
由图1、图2可知,稀盐酸与稀氢氧化钠已发生中和反应的判断依据是 .
(2)对于某些有明显实验现象产生的中和反应,如稀硫酸与氢氧化钡溶液的反应,只要将稀硫酸滴加到氢氧化钡溶液中,观察到 现象,就可说明反应已经发生.该反应的化学方程式是 .
考点:
中和反应及其应用;书写化学方程式、文字表达式、电离方程式.
专题:
常见的酸 酸的通性.
分析:
(1)显酸性的溶液不能使酚酞试液变色,显碱性的溶液能使酚酞试液变红色;
稀盐酸和氢氧化钠反应时放出热量;
氢氧化钠溶液显碱性,pH大于7,当不断加入稀盐酸时,由于发生中和反应,溶液的碱性减弱,pH减小,当恰好完全反应时,pH等于7,继续加入稀盐酸时,溶液显酸性,pH小于7;
氢氧化钡和稀硫酸反应生成白色沉淀硫酸钡和水.
解答:
解:(1)①在盛有稀氢氧化钠溶液的烧杯中,滴加2~3滴酚酞试液,用胶头滴管吸取稀盐酸逐滴加入到上述烧杯中,边滴边用玻璃棒搅拌,当观察到溶液由红色变成无色时,说明它们之间发生了中和反应,且恰好完全反应;
②由图1、图2可知,稀盐酸与稀氢氧化钠已发生中和反应的判断依据是溶液温度升高;溶液pH由大于7降至小于7.
故填:溶液由红色变成无色;溶液温度升高;溶液pH由大于7降至小于7.
(2)将稀硫酸滴加到氢氧化钡溶液中时,能够观察到产生白色沉淀,就可说明反应已经发生,该反应的化学方程式为:Ba(OH)2+H2SO4═BaSO4↓+2H2O.
故填:产生白色沉淀;Ba(OH)2+H2SO4═BaSO4↓+2H2O.
点评:
实验现象是物质之间相互作用的外在表现,因此要学会设计实验、观察实验、分析实验,为揭示物质之间相互作用的实质奠定基础.

下列说法正确的是( )
|
| A. | 向酸性土壤里撒熟石灰,可调节土壤的pH |
|
| B. | 推广加碘盐是为了预防胃酸过多 |
|
| C. | 钢铁在干燥的环境中比在潮湿的环境中更容易被腐蚀 |
|
| D. | 玻璃钢、光导纤维和合成纤维都是有机合成材料 |
室温时,将氢氧化钠溶液与盐酸用滴加方式反应时,溶液的pH随滴入溶液体积变化如图所示.下列有关说法不正确的是( )
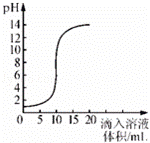
|
| A. | 该图象表示的是将氢氧化钠溶液滴入盐酸中 |
|
| B. | 氢氧化钠溶液和盐酸恰好完全反应时.溶液的pH等于7 |
|
| C. | 当滴入溶液的体积为5mL时,所得溶液中的溶质只有NaCl |
|
| D. | 滴入溶液体积为15mL时,再加几滴紫色石蕊试液溶液呈蓝色 |
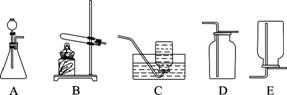 (1)A装置可用于制(填气体名称)____,反应的化学方程式为:____。
(1)A装置可用于制(填气体名称)____,反应的化学方程式为:____。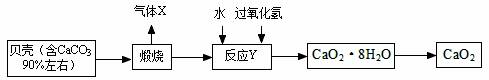
 2CaO+O2↑+16H2O↑,杂质不发生变化),测得生成氧气的质量为3.2g,请计算样品中CaO2·8H2O的质量分数(CaO2·8H2O相对分子质量为216),写出必要的计算过程。
2CaO+O2↑+16H2O↑,杂质不发生变化),测得生成氧气的质量为3.2g,请计算样品中CaO2·8H2O的质量分数(CaO2·8H2O相对分子质量为216),写出必要的计算过程。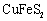 )产生硫酸盐,进而生产铜和绿矾,主要流程如下:
)产生硫酸盐,进而生产铜和绿矾,主要流程如下:
