题目内容
13.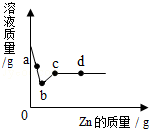 向一定质量AgNO3和Cu(NO3)2的混合溶液中加入Zn,溶液质量与加入Zn的质量关系如图所示.下列说法不正确的是( )
向一定质量AgNO3和Cu(NO3)2的混合溶液中加入Zn,溶液质量与加入Zn的质量关系如图所示.下列说法不正确的是( )| A. | b点溶液中溶质没有AgNO3 | |
| B. | c点溶液中溶质为Zn(NO3)2 | |
| C. | 若取b~c段固体,滴加稀盐酸,无气泡产生 | |
| D. | d点的固体有2种 |
分析 根据金属与盐溶液的反应进行分析,在金属活动性顺序中,位置在前的金属能将位于其后的金属从其盐溶液中置换出来,且置换时先把最弱的金属置换出来,并通过各反应的关系进行溶液质量的变化分析.
解答 解:在金属活动性顺序中,Zn>Cu>Ag,向一定质量AgNO3和Cu(NO3)2的混合溶液中加入Zn,与两种溶质依次发生反应
Zn+2AgNO3=Zn(NO3)2+2Ag
65 216
所以析出银的过程是溶液质量减少的过程;
Zn+Cu(NO3)2=Zn(NO3)2+Cu
65 64
所以析出铜的过程是溶液质量增加的过程
A、b点是硝酸银恰好被反应完,故b点溶液中溶质没有AgNO3,故A说法正确;
B、c点时硝酸铜恰好完全反应,溶液中只有硝酸锌,得到的固体是银和铜两种,故b说法正确;
C、b~c段是硝酸银全部参加反应完后锌和硝酸铜反应的过程,固体为银和铜,滴加稀盐酸,无气泡产生,故C说法正确;
D、d点时锌过量,得到的固体是银和铜、锌,故D说法错误;
故选D.
点评 本题考查了金属活动性顺序的应用,要求学生熟悉金属的活动性顺序表,能利用活动性判断反应的发生,还要结合坐标分析各段的意义.

练习册系列答案
相关题目
3.下列化学方程式中,书写正确的是( )
| A. | 2H2O═2H2↑+O2 | B. | H2SO4+NaOH═NaSO4+H2O | ||
| C. | 2KMnO4$\frac{\underline{\;\;△\;\;}}{\;}$K2MnO4+MnO2+O2↑ | D. | Fe+HC1=FeCl2+H2↑ |
1.对于下列化学用语,有关说法正确的是( )
①H2 ②Na+ ③CO2 ④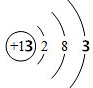 ⑤$\stackrel{+2}{Mg}$Cl2.
⑤$\stackrel{+2}{Mg}$Cl2.
①H2 ②Na+ ③CO2 ④
 ⑤$\stackrel{+2}{Mg}$Cl2.
⑤$\stackrel{+2}{Mg}$Cl2.| A. | ①可表示2个氢原子 | |
| B. | ②和④可表示阳离子 | |
| C. | ③中碳元素的化合价为+4价 | |
| D. | ⑤中“+2”表示在氯化镁中镁离子带两个单位的正电荷 |
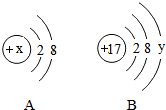 A、B两种微粒结构示意图如图所示.根据图示回答下列问题:
A、B两种微粒结构示意图如图所示.根据图示回答下列问题: 黄铜是铜锌合金,它用于制造机器、电器零件等,为测定黄铜样品中铜的质量分数,取10g该样品粉碎,加入足量的溶质质量分数为10%的稀盐酸,反应情况如图所示,求:
黄铜是铜锌合金,它用于制造机器、电器零件等,为测定黄铜样品中铜的质量分数,取10g该样品粉碎,加入足量的溶质质量分数为10%的稀盐酸,反应情况如图所示,求: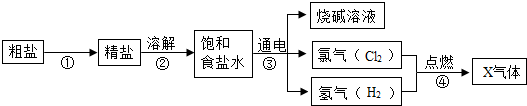
 钙是维持人体正常功能所必需的元素,如图所示为某种补钙剂“钙尔奇”说明书的一部分,取一片钙尔奇,放入盛有10g稀盐酸的烧杯中,其中碳酸钙跟盐酸恰好完全反应(其它成分与盐酸不反应),烧杯内物质质量变为11.34g,试计算钙尔奇中碳酸钙的质量分数.
钙是维持人体正常功能所必需的元素,如图所示为某种补钙剂“钙尔奇”说明书的一部分,取一片钙尔奇,放入盛有10g稀盐酸的烧杯中,其中碳酸钙跟盐酸恰好完全反应(其它成分与盐酸不反应),烧杯内物质质量变为11.34g,试计算钙尔奇中碳酸钙的质量分数.