题目内容
在48g水中加入20g质量分数为10%的氢氧化钠溶液,(氢氧化钠溶液只是增强水的导电性)通直流电反应一段时间后,剩余溶液的质量为50g.计算:
(1)通电后产生的氧气的质量;
(2)剩余溶液中氢氧化钠的质量分数.
设通电后产生的氧气的质量为x.
2H2O
 2H2↑+O2↑
2H2↑+O2↑36 32
18g x
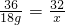
x=16g
(2)剩余溶液中氢氧化钠的质量分数=
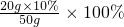 =4%
=4%答:(1)通电后产生的氧气的质量为16g;
(2)剩余溶液中氢氧化钠的质量分数为20%.
分析:(1)根据反应的化学方程式,减少的质量就是参加反应水的质量,由水的质量可计算产生的氧气的质量;
(2)由于反应前后氢氧化钠质量不变,改变的只是溶液中水的质量,由氢氧化钠质量与所剩余溶液的质量比,可计算电解水后的氢氧化钠溶液的质量分数.
点评:根据反应的化学方程式可以表示反应中各物质的质量比,由反应中某物质的质量可计算反应中其它物质的质量.

 名校课堂系列答案
名校课堂系列答案溶液在生命活动和生产生活、科学实验中起着十分重要的作用。
(1)硫酸铜溶液中的溶剂为 。
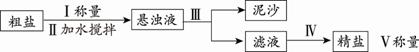
(2)提纯含少量泥沙的粗盐,一般经过以下操作流程:
 |
① 操作III的名称为 。
② 操作IV中为尽量减少飞溅,可以采取的措施是 。
③ 精盐和粗盐质量的比值为产率。下列操作会造成产率偏低的是 (填字母序号)。
A.食盐没有全部溶解即过滤 B.蒸发时飞溅剧烈
C.蒸发后,所得精盐潮湿 D.蒸发后所得精盐未全部转移到称量纸上
(3)某同学利用实验探究NaCl在水中的溶解限度,所得数据记录如下。
| 序号 | 温度 | 水质量 | NaCl质量 | |
| 加入 | 未溶 | |||
| ① | 20℃ | 25g | 9g | 0 |
| ② | 20℃ | 50g | 20g | 2g |
| ③ | 20℃ | 100g | 34g | 0 |
| ④ | 20℃ | 125g | 48g | 3g |
| ⑤ | 20℃ | 150g | 54g | 0 |
上述实验中,所得溶液为饱和溶液的是 (填数字序号)。
溶液在生命活动和生产生活、科学实验中起着十分重要的作用。
(1)硫酸铜溶液中的溶质为 。
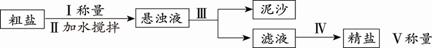
(2)提纯含少量泥沙的粗盐,一般经过以下操作流程:
 |
① 操作 Ⅲ和Ⅳ的名称分别为 、 。
Ⅲ和Ⅳ的名称分别为 、 。
② 精盐和粗盐质量的比值为产率。下列操作会造成产率偏低的是:
(填字母序号)。
 A.食盐没有全部溶解即过滤 B.蒸发时飞溅剧烈
A.食盐没有全部溶解即过滤 B.蒸发时飞溅剧烈
C.蒸发后,所得精盐潮湿 D.蒸发后所得精盐未全部转移到称量纸上
(3)某同学利用实验探究NaCl在水中的溶解限度,所得数据记录如下。
| 序号 | 温度 | 水的质量 | NaCl质量 | |
| 加入 | 未溶 | |||
| ① | 20℃ | 25g | 9g | 0 |
| ② | 20℃ | 50g | 20g | 2g |
| ③ | 20℃ | 100g | 34g | 0 |
| ④ | 20℃ | 125g | 48g | 3g |
| ⑤ | 20℃ | 150g | 54g | 0 |
上述实验中,所得溶液为饱和溶液的是 (填数字序号)。

