题目内容
8.取10g碳酸钙高温加热一段时间后停止加热,测得剩余固体的质量为8g,则下列判断不正确的是( )| A. | 生成了2g二氧化碳 | B. | 该变化符合质量守恒定律 | ||
| C. | 生成了5.6g氧化钙 | D. | 剩余固体中钙元素的质量为4g |
分析 结合质量守恒定律可以知道,反应前后固体质量之差为二氧化碳的质量,在反应前后钙元素的质量相等,所以反应后剩余物质中钙元素的质量即为反应前碳酸钙中钙元素的质量,可以据此进行解答.
解答 解:根据质量守恒定律可以知道生成二氧化碳的质量为:10.0g-8.0g=2.0g;
根据题意可以知道钙元素的质量为:10.0g×$\frac{40}{40+12+16×3}×100%$=4.0g;
设生成氧化钙的质量为x
CaCO3 $\frac{\underline{\;高温\;}}{\;}$CaO+CO2↑
56 44
x 2.0g
$\frac{56}{44}=\frac{x}{2g}$
x=2.55g
A、生成了2g二氧化碳,正确;
B、该变化符合质量守恒定律,正确;
C、生成了22.55g氧化钙,错误;
D、剩余固体中钙元素的质量为4g,正确.
故选C.
点评 考点考查了根据化学方程式的计算,是中考计算题中经常出现的题型.做题时要注意:化学方程式要写正确,始终不要忘记质量守恒定律,还要记牢“遇到差值要想气体”.

练习册系列答案
相关题目
3.2014年2月11日徐州一市民取暖不当,引发火灾.下列措施存在火灾隐患的是( )
| A. | 进入未知山洞深处要点火把 | B. | 发现燃气泄漏,点火检查出泄漏处 | ||
| C. | 炒菜油锅着火,用锅盖盖灭火焰 | D. | 点燃氢气前要检验氢气的纯度 |
13.化学是创造物质的科学,要创造新物质,其核心是认识物质的微观结构和变化规律.下列关于物质微观结构的说法中,不正确的是( )
| A. | 原子既可以变成离子构成物质,也可以结合成分子构成物质,但不能直接构成物质 | |
| B. | 分子很小,但既有质量,又有能量 | |
| C. | 原子在化学变化中的表现主要取决于原子的最外层电子 | |
| D. | 原子都是由更小的粒子构成的 |
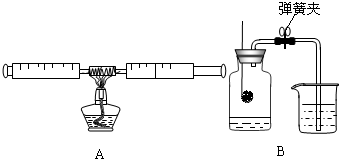 小红用如图所示的A装置测定空气中氧气的含量.硬质玻璃管内装有细铜丝,且两个注射器组成的密闭系统内留有30mL室温下的空气.回答下列问题:
小红用如图所示的A装置测定空气中氧气的含量.硬质玻璃管内装有细铜丝,且两个注射器组成的密闭系统内留有30mL室温下的空气.回答下列问题: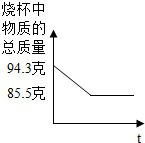 为测定石灰石样品中碳酸钙的质量分数,某学习小组进行了如下实验探究,取25g石灰石样品放入烧杯中,加入稀盐酸至不再产生气泡为止(石灰石中的杂质不溶于水,也不与水反应),并绘制了烧杯中物质的总质量与时间的坐标图(如图所示).
为测定石灰石样品中碳酸钙的质量分数,某学习小组进行了如下实验探究,取25g石灰石样品放入烧杯中,加入稀盐酸至不再产生气泡为止(石灰石中的杂质不溶于水,也不与水反应),并绘制了烧杯中物质的总质量与时间的坐标图(如图所示). 在公共场所有如图所示的广告.请回答下列问题:
在公共场所有如图所示的广告.请回答下列问题: