题目内容
5.下列A→D的实验装置进行合理组合,即可制取二氧化碳气体也可制取氧气.
(1)写出标注①的仪器名称酒精灯.
(2)实验室用A装置制取氧气时,在分液漏斗中添加的药品是H2O2(填化学式),用排水法收集氧气,观察到气泡连续均匀放出时,再将注满水的集气瓶倒扣住导气管,收集氧气.若用加热分解高锰酸钾的方法制取氧气,则选用的发生装置为B(填标号),该反应的化学方程式为2KMnO4$\frac{\underline{\;\;△\;\;}}{\;}$K2MnO4+MnO2+O2↑.
(3)用A、D装置制取并收集二氧化碳,仪器接口的连接顺序是a→c(填“b”或“c”).若在D中装半瓶氢氧化钠溶液,将A中生成的二氧化碳气体通入其中一会儿,肉眼观察不到什么可见现象.实验小组将进行如下三个实验探究活动,用实验的方法证明二氧化碳与氢氧化钠发生了反应,并验证产物碳酸钠.
实验一:取反应后的D中溶液,滴加酚酞试剂,溶液变红.
实验二:取反应后的D中溶液,加几滴稀盐酸,未观察到气泡的产生.
实验三:取反应后的D中溶液,滴加澄清石灰水,出现浑浊.
(4)研究表明,实验一不能证明化学反应是否进行,理由是氢氧化钠和碳酸钠溶液都呈碱性.
(5)请判断实验二能否证明变红中无碳酸钠生成并说明理由不能,反应后D中溶液氢氧化钠过量,会与稀盐酸反应.
(6)写出实验三发生变红的化学反应方程式Ca(OH)2+Na2CO3=CaCO3↓+2NaOH.
查资料:常温下,氢氧化钠易溶于酒精溶剂形成溶液,而碳酸钠难溶于酒精溶剂.
(7)请你根据“资料”信息,设计一个实验方案,证明二氧化碳与氢氧化钠发生了化学反应将二氧化碳通入氢氧化钠酒精溶液中,能观察到有不溶性物质生成.
(8)若以上方案有人用75%的医用酒精来配制氢氧化钠溶液进行实验,结果达不到预期效果,原因是75%的酒精溶液中含有水,碳酸钠会溶于水.
分析 酒精灯是常用的加热仪器,制取装置包括加热和不需加热两种,如果用双氧水和二氧化锰制氧气就不需要加热,如果用高锰酸钾或氯酸钾制氧气就需要加热.氧气的密度比空气的密度大,不易溶于水,因此能用向上排空气法和排水法收集.实验室制取CO2,是在常温下,用大理石或石灰石和稀盐酸制取的,碳酸钙和盐酸互相交换成分生成氯化钙和水和二氧化碳,因此不需要加热.二氧化碳能溶于水,密度比空气的密度大,因此只能用向上排空气法收集.研究表明,实验一不能证明化学反应是否进行,理由是:氢氧化钠和碳酸钠溶液都呈碱性;实验二不能证明无碳酸钠生成,因为反应后D中溶液氢氧化钠过量,会与稀盐酸反应;氢氧化钙和碳酸钠反应生成碳酸钙白色沉淀和氢氧化钠,因为有氢氧化钠生成,所以变红;二氧化碳与氢氧化钠发生了化学反应的属于方案:将二氧化碳通入氢氧化钠酒精溶液中,能观察到有不溶性物质生成;若以上方案有人用75%的医用酒精来配制氢氧化钠溶液进行实验,结果达不到预期效果,原因是:75%的酒精溶液中含有水,碳酸钠会溶于水.
解答 解:(1)酒精灯是常用的加热仪器,故答案为:酒精灯;
(2)如果用双氧水和二氧化锰制氧气就不需要加热,在分液漏斗中添加的药品是过氧化氢溶液;用排水法收集氧气,观察到:气泡连续均匀放出时,再将注满水的集气瓶倒扣住导气管,收集氧气;如果用高锰酸钾制氧气就需要加热,高锰酸钾受热分解生成锰酸钾和二氧化锰和氧气,要注意配平;故答案为:H2O2;气泡连续均匀放出;B;2KMnO4$\frac{\underline{\;\;△\;\;}}{\;}$K2MnO4+MnO2+O2↑;
(3)用A、D装置制取并收集二氧化碳,仪器接口的连接顺序是a→c,因为二氧化碳的密度比空气大;故答案为:c;
(4)研究表明,实验一不能证明化学反应是否进行,理由是:氢氧化钠和碳酸钠溶液都呈碱性;故答案为:氢氧化钠和碳酸钠溶液都呈碱性;
(5)实验二不能证明无碳酸钠生成,因为反应后D中溶液氢氧化钠过量,会与稀盐酸反应;故答案为:不能,反应后D中溶液氢氧化钠过量,会与稀盐酸反应;
(6)氢氧化钙和碳酸钠反应生成碳酸钙白色沉淀和氢氧化钠,因为有氢氧化钠生成,所以变红;故答案为:Ca(OH)2+Na2CO3=CaCO3↓+2NaOH;
(7)二氧化碳与氢氧化钠发生了化学反应的属于方案:将二氧化碳通入氢氧化钠酒精溶液中,能观察到有不溶性物质生成;故答案为:将二氧化碳通入氢氧化钠酒精溶液中,能观察到有不溶性物质生成;
(8)若以上方案有人用75%的医用酒精来配制氢氧化钠溶液进行实验,结果达不到预期效果,原因是:75%的酒精溶液中含有水,碳酸钠会溶于水;故答案为:75%的酒精溶液中含有水,碳酸钠会溶于水;
点评 本考点主要考查了仪器的名称、气体的制取装置和收集装置的选择,同时也考查了化学方程式的书写和实验探究等,综合性比较强.气体的制取装置的选择与反应物的状态和反应的条件有关;气体的收集装置的选择与气体的密度和溶解性有关.本考点是中考的重要考点之一,主要出现在实验题中.

 亮点激活精编提优100分大试卷系列答案
亮点激活精编提优100分大试卷系列答案| A. | 水可溶解任何物质 | |
| B. | 硬水通过活性炭吸附可变成软水 | |
| C. | 生活污水危害不大,可任意排放 | |
| D. | 电解水实验证明水是由氢元素和氧元素组成 |
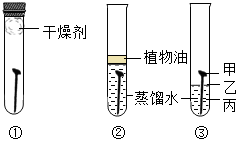 某小组为探究铁钉锈蚀的条件,设计实验如图所示.下列说法正确的是( )
某小组为探究铁钉锈蚀的条件,设计实验如图所示.下列说法正确的是( )| A. | ①和③对比,证明铁钉锈蚀需要氧气 | |
| B. | ②中植物油的作用是防止水蒸发 | |
| C. | ③中铁钉的甲、乙、丙三处,丙处锈蚀最严重 | |
| D. | 实验证明了铁在潮湿空气中容易生锈 |
| A. | 原子的质子数不同 | B. | 原子的电子数不同 | ||
| C. | 原子的中子数不同 | D. | 原子的最外层电子数不同 |
| A. | 对二甲苯由碳原子和 氢原子构成 | |
| B. | 对二甲苯的相对分子质量为106g | |
| C. | 对二甲苯充分燃烧的产物是二氧化碳和水 | |
| D. | 对二甲苯中碳、氢元素的质量比为4:5 |
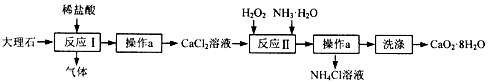
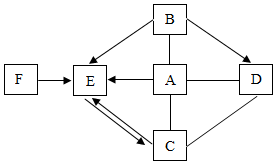 如图所示A~F是初中化学常见的物质.图中“→”表示转化关系,“-”表示相互能反应(部分物质和反应条件未标出).其中A是人体胃液中含有的酸,A和B发生中和反应可得到生活中常用的一种调味品,固体C常用于改良酸性土壤.
如图所示A~F是初中化学常见的物质.图中“→”表示转化关系,“-”表示相互能反应(部分物质和反应条件未标出).其中A是人体胃液中含有的酸,A和B发生中和反应可得到生活中常用的一种调味品,固体C常用于改良酸性土壤.