题目内容
14.化学科代表和小明同学帮助老师整理化学药品时,他们发现分别放在两个试剂瓶中的两片用砂纸磨得磨得光亮的银白色金属,未贴标签.它们可能是哪两种金属?它们的金属活动性谁强?两位同学想对这两种金属X和Y的金属活动性顺序进行实验探究.(1)进行猜想:①科代表猜想:活动性X大于Y.②小明同学猜想:X小于Y
(2)探究实验:请你完成实验报告的空白内容
| 实验步骤 | 实验现象 | 结论 |
| 将金属X和Y分别放入稀盐酸中 | 金属Y表面无明显变化,金属X的表面有气泡冒出.将燃着的木条放在装金属X的试管口,气体燃烧 | 科代表同学猜想是正确的 |
分析 (1)活动性可能是X大于Y,也可能是X小于Y;
(2)比较活泼的金属能和稀盐酸、稀硫酸反应生成氢气和盐,比较不活泼的金属不能和稀盐酸、稀硫酸反应;
(3)铁比较活泼,能和稀盐酸反应生成氯化亚铁和氢气,银不活泼,不能和稀盐酸反应.
解答 解:(1)进行猜想:①课代表猜想:活动性X大于Y.②小明同学猜想:X小于Y.
故填:X小于Y.
(2)将金属X和Y分别放入稀盐酸中,金属Y表面无明显变化,说明Y不活泼,金属X的表面有气泡冒出,将燃着的木条放在装金属X的试管口,气体燃烧,说明X比较活泼,能和稀盐酸反应生成盐和氢气,因此课代表的猜想是正确的,实验过程如下表所示:
| 实验步骤 | 实验现象 | 结论 |
| 将金属X和Y分别放入稀盐酸中 | 金属Y表面无明显变化,金属X的表面有气泡冒出.将燃着的木条放在装金属X的试管口,气体燃烧 | 科代表同学猜想是正确的 |
故填:银.
点评 要会利用金属活动顺序表分析实验,氢前边的金属会与稀硫酸、盐酸反应,但氢后边的金属不会与稀硫酸、盐酸反应,前边的金属会把后边的金属从其盐溶液中置换出来.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
5. 化学兴趣小组同学进行中和反应实验时,将4mL2%的稀硫酸逐滴滴加到2mL2%的氢氧化钠溶液中,测得溶液的pH变化曲线如图所示.
化学兴趣小组同学进行中和反应实验时,将4mL2%的稀硫酸逐滴滴加到2mL2%的氢氧化钠溶液中,测得溶液的pH变化曲线如图所示.
【提出问题】导致溶液pH变化的原因是什么?
【查阅资料】(1)溶液的pH是由H+或OH-浓度决定,H+浓度越大,
pH越小;OH-浓度越大,pH越大.
(2)溶液中某种离子浓度非常小时,可忽略不计.
【作出猜想】猜想①:溶液pH变化是因为氢氧化钠溶液被稀释.
猜想②:溶液pH变化是因为发生了化学反应.
【进行实验】同学们分成两组分别进行实验.
甲组:同学们将4mL2%的稀硫酸换成4mL水,逐滴滴加到2mL2%的氢氧化钠溶液中,并测得溶液的pH始终大于7,说明猜想Ⅰ不合理.
乙组:同学们分别取a、b、c三处溶液进行实验.
【实验结论】猜想Ⅱ合理.
【知识拓展】从微观角度分析,中和反应的实质是H+和OH-反应变成H2O.
 化学兴趣小组同学进行中和反应实验时,将4mL2%的稀硫酸逐滴滴加到2mL2%的氢氧化钠溶液中,测得溶液的pH变化曲线如图所示.
化学兴趣小组同学进行中和反应实验时,将4mL2%的稀硫酸逐滴滴加到2mL2%的氢氧化钠溶液中,测得溶液的pH变化曲线如图所示.【提出问题】导致溶液pH变化的原因是什么?
【查阅资料】(1)溶液的pH是由H+或OH-浓度决定,H+浓度越大,
pH越小;OH-浓度越大,pH越大.
(2)溶液中某种离子浓度非常小时,可忽略不计.
【作出猜想】猜想①:溶液pH变化是因为氢氧化钠溶液被稀释.
猜想②:溶液pH变化是因为发生了化学反应.
【进行实验】同学们分成两组分别进行实验.
甲组:同学们将4mL2%的稀硫酸换成4mL水,逐滴滴加到2mL2%的氢氧化钠溶液中,并测得溶液的pH始终大于7,说明猜想Ⅰ不合理.
乙组:同学们分别取a、b、c三处溶液进行实验.
| 实验操作 | 实验现象 | 实验分析 |
| 取适量a处溶液于试管中,加入镁条 | 无气泡产生 | 溶液中几乎不含H+(填离子符号) |
| 取适量b处溶液于试管中,加入紫色石蕊溶液 | 石蕊溶液不变色 | 溶液中几乎不含H+和OH- |
| 取适量c处溶液于试管中,加入硫酸铜溶液 | 无沉淀产生 | 溶液中几乎不含OH- |
【知识拓展】从微观角度分析,中和反应的实质是H+和OH-反应变成H2O.
2.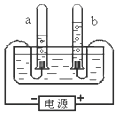 根据所学知识,我们可以从“电解水实验”中获得更多的信息和推论.下列说法正确的是( )
根据所学知识,我们可以从“电解水实验”中获得更多的信息和推论.下列说法正确的是( )
 根据所学知识,我们可以从“电解水实验”中获得更多的信息和推论.下列说法正确的是( )
根据所学知识,我们可以从“电解水实验”中获得更多的信息和推论.下列说法正确的是( )| A. | 水是由氢气和氧气组成的 | |
| B. | 试管b中所得气体能燃烧 | |
| C. | 试管a、b中所得气体的质量比约为2:1 | |
| D. | 试管a、b中所得气体的体积比约为2:1 |
9.某学生用量筒量取液体的体积,量筒放平且面对刻度线,先仰视凹液面的最低点读数为19mL;倾出部分液体后,俯视液体凹液面的最低处读数为10mL,则实际该学生倾出液体的体积( )
| A. | 等于9mL | B. | 大于9mL | C. | 小于9mL | D. | 无法判断 |
19.如果植株生长得特别矮小,而且叶片呈暗绿色甚至紫色,是由于缺少哪种无机盐( )
| A. | 氮 | B. | 磷 | C. | 钾 | D. | 铁 |
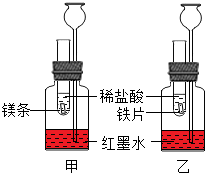 探究活动一:在室温条件下进行如图所示实验.已知:试管内的镁条和铁片表面均被打磨洁净,且形状、大小均相同;同时加入两支试管中的稀盐酸的质量和质量分数均相等.
探究活动一:在室温条件下进行如图所示实验.已知:试管内的镁条和铁片表面均被打磨洁净,且形状、大小均相同;同时加入两支试管中的稀盐酸的质量和质量分数均相等.