题目内容
15、镁在空气中燃烧生成氧化镁和氮化镁(其中氮为-3价),已知氮化镁是黄绿色固体,根据镁条在空气中燃烧的实验现象,可知在这样的条件下,镁更易与
O2
(填O2或N2)化合,理由是
生成白色固体
.这一现象证明
O2
的化学性质更活泼.分析:镁条在空气中燃烧,发出耀眼白光,放出大量的热,生成一种白色固体,而氮化镁是黄绿色固体,说明镁在空气中燃烧主要与空气中的氧气发生反应.空气中氮气的体积分数为78%、氧气为21%,空气中氮气含量远大于氧气.
解答:解:虽然空气中氮气含量要大于氧气,但是镁条在空气中燃烧生成白色固体氧化镁而非黄色的氮化镁,这说明镁更易与氧气反应;这是由于氧气是一种化学性质活泼的气体,而氮气的化学性质不活泼,较难与其它物质发生反应;
故答案为:O2;生成白色固体;O2.
故答案为:O2;生成白色固体;O2.
点评:氧气是一种化学性质比较活泼的气体,能与许多物质发生氧化反应;而氮气的化学性质不活泼,通常情况下不与其它物质发生反应.

练习册系列答案
 品学双优卷系列答案
品学双优卷系列答案 小学期末冲刺100分系列答案
小学期末冲刺100分系列答案 期末复习检测系列答案
期末复习检测系列答案
相关题目
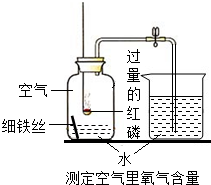 学习了空气中氧气的含量测定后,化学兴趣小组的同学对过量的红磷能否消耗完瓶中的氧气表示有疑问.请你参与他们的探究活动,并回答下列的问题:
学习了空气中氧气的含量测定后,化学兴趣小组的同学对过量的红磷能否消耗完瓶中的氧气表示有疑问.请你参与他们的探究活动,并回答下列的问题:

 15、镁在空气中燃烧,生成氧化镁,其固体质量变化如右图所示,则 固(80-48)g表示的质量是
15、镁在空气中燃烧,生成氧化镁,其固体质量变化如右图所示,则 固(80-48)g表示的质量是