题目内容
1.七水硫酸镁(MgSO4•7H2O)是一种重要的化工原料,在48.1℃以下的潮湿空气中稳定,在温热干燥空气中易失去结晶水.工业上将白云石(主要成分为MgCO3、CaCO3)煅烧成粉,用于制取MgSO4•7H2O,工艺流程如下图所示: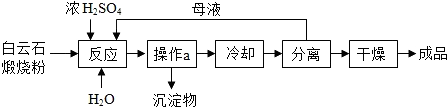
(1)煅烧过程中,MgCO3转化为MgO的基本反应类型是分解反应.
(2)写出MgO与H2SO4反应的化学方程式MgO+H2SO4=MgSO4+H2O.
(3)操作a的名称为过滤.
(4)将分离后的母液循环利用的目的是提高原料的利用率.
(5)干燥得成品时,需要控制的条件是温度.
分析 (1)根据碳酸镁煅烧反应生成氧化镁和二氧化碳进行解答;
(2)根据碳酸镁和硫酸反应生成硫酸镁、水和二氧化碳进行解答;
(3)根据过滤操作可用于分离难溶性固体进行解答;
(4)根据结晶后的母液是MgSO4的饱和溶液,循环利用母液可使原料中的镁元素最大可能地转化到产物中进行解答;
(5)根据七水硫酸镁在湿热干燥空气中易失去结晶水进行解答.
解答 解:(1)碳酸镁煅烧反应生成氧化镁和二氧化碳,是一种物质反应生成两种物质,属于分解反应;
(2)碳酸镁和硫酸反应生成硫酸镁、水和二氧化碳,化学方程式为:MgO+H2SO4=MgSO4+H2O;
(3)操作a是过滤操作;
(4)结晶后的母液是MgSO4的饱和溶液,循环利用母液可使原料中的镁元素最大可能地转化到产物中,因此将分离后的母液循环利用的目的是提高原料的利用率;
(5)由于七水硫酸镁在湿热干燥空气中易失去结晶水,因此干燥得成品时,需要控制的条件是温度,以防止七水硫酸镁水解.
故答案为:(1)分解反应;(2)MgO+H2SO4=MgSO4+H2O;(3)过滤;(4)提高原料的利用率;(5)温度.
点评 本题考查了物质分离的实验设计和方法应用,主要是利用硫酸除去杂质,得到较纯净的MgSO4溶液来制备MgSO4•7H2O晶体,同时考查了物质分离方法,题目难度中等.

练习册系列答案
 名师伴你成长课时同步学练测系列答案
名师伴你成长课时同步学练测系列答案
相关题目
9.205年一些大城市雾霾天气仍然非常严重,形成雾霾天气的原因是空气中PM2.5含量的增加,PM2.5指的是( )
| A. | SO2 | B. | 可吸入颗粒物 | C. | NO2 | D. | CO |
16.在一密闭容器中,甲、乙、丙、丁四种物质反应前后的质量如下,下列说法正确的是( )
| 物质 | 甲 | 乙 | 丙 | 丁 |
| 反应前质量/g | 20 | 6 | 20 | 22 |
| 反应后质量/g | 2 | 待测 | 32 | 28 |
| A. | 该反应是化合反应 | B. | 甲、丙在反应中的质童比为2:3 | ||
| C. | “待测”为6g | D. | 乙在该反应中一定是催化剂 |
13.张丽同学用托盘天平称量12.4g药品,在称量中发现指针向左偏转,你给她的正确建议是( )
| A. | 减少药品 | B. | 移动游码 | ||
| C. | 向右盘中加砝码 | D. | 调节天平的平衡螺母 |
11.等质量的氢气、甲烷和一氧化碳完全燃烧需要氧气的质量( )
| A. | CO最多,H2最少 | B. | H2最多,CH4最少 | C. | H2最多,CO最少 | D. | CH4最多,CO最少 |