题目内容
5.下列装置常用于实验室制取气体.根据给出的装置回答下列问题: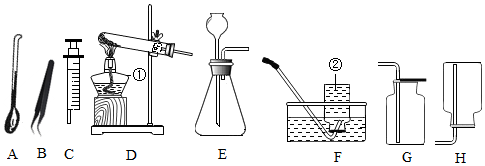
(1)指出编号仪器名称:①酒精灯;
(2)实验室用加热高锰酸钾制取氧气,制取并收集较纯净的氧气所有装置是D、F(从A~H中选择),反应原理用化学方程式表示为2KMnO4$\frac{\underline{\;\;△\;\;}}{\;}$K2MnO4+MnO2+O2↑,实验中待气泡连续均匀地冒出时收集氧气比较适宜;
(3)制取并收集二氧化碳应选择的装置是E、G(从A~H中选择),实验中需要控制产生二氧化碳速率,改进的方法是把E装置中的长颈漏斗改为C(从A~H中选择).
分析 (1)认识常规仪器熟悉其基本用途和注意事项;
(2)高锰酸钾受热制取氧气,是固体加热制备气体,要得到较为纯净的气体则应该选用排水法收集,若要制备干燥的则采用排空气法或者,排水法收集的最佳时机是气泡连续均匀冒出的时候,前期的气体可能是装置内的空气受热而溢出,或者是生成的气体混合着装置内的空气而溢出;
(3)二氧化碳制取是固体和液体常温下反应,所以发生装置只有E可选.控制反应速率,一是改变颗粒大小,二是改变液体滴加速率,控制速率可以采用注射器或者是分液漏斗.
解答 解:(1)仪器①名称是酒精灯;
(2)实验室用加热高锰酸钾制取氧气,用加热固体装置,收集较纯净的氧气用排水法收集,制取并收集较纯净的氧气所有装置是D、F,反应原理用化学方程式表示为2KMnO4$\frac{\underline{\;\;△\;\;}}{\;}$ K2MnO4+MnO2+O2↑,实验中待气泡连续均匀地冒出时收集氧气比较适宜;
(3)实验室常温下用大理石与稀盐酸反应制取二氧化碳,固体与液体常温下反应,发生装置用E,二氧化碳密度比空气大且能溶于水,只能用向上排空气法收集,收集二氧化碳应选择的装置是G,制取并收集二氧化碳应选择的装置是E、G,实验中需要控制产生二氧化碳速率,可以用分液漏斗或注射剂加入稀盐酸,改进的方法是把E装置中的长颈漏斗改为C.
故答案为:(1)酒精灯;(2)D、F 2KMnO4$\frac{\underline{\;\;△\;\;}}{\;}$ K2MnO4+MnO2+O2↑,气泡连续均匀地冒出;(3)E、G,长颈漏斗 C
点评 反应速率的控制可以从反应物浓度、反应物的接触面积(颗粒大小、浓度高度),也可以考虑控制滴加的速率来实现.

练习册系列答案
 核心素养学练评系列答案
核心素养学练评系列答案 单元期中期末卷系列答案
单元期中期末卷系列答案
相关题目
15.下列有关水的说法正确的是( )
| A. | 煮沸可以使硬水软化 | B. | 地球上的淡水资源非常丰富 | ||
| C. | 水可以溶解任何物质 | D. | 水是由氢气和氧气组成的 |
16.下列实验操作正确的是( )
| A. | 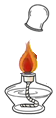 | B. | 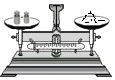 | C. | 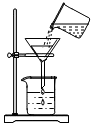 | D. | 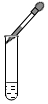 |
17.正确的实验操作对实验结果、人身安全都非常重要,下列实验操作正确的是( )
| A. | 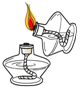 点燃酒精灯 | B. | 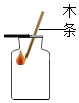 氧气验满 | C. | 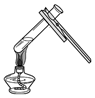 液体加热 | D. | 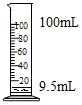 量9.5mL液体 |
14.我们的衣、食、住、行无不与化学材料有关,我们生活在化学世界里.教室中的下列物品由天然材料制成的是( )
| A. | 玻璃 | B. | 铝合金门窗 | C. | 木制桌凳 | D. | 陶瓷地板 |
 某实验小组同学用如图所示装置进行空气中氧气含量的测定,其中集气瓶的容积为250mL.
某实验小组同学用如图所示装置进行空气中氧气含量的测定,其中集气瓶的容积为250mL. 已知A、B、C、D、X、Y、Z均为初中化学常见的物质,相互关系如图所示,“→”表示转化关系,“-”表示相互之间能反应(部分反应物、
已知A、B、C、D、X、Y、Z均为初中化学常见的物质,相互关系如图所示,“→”表示转化关系,“-”表示相互之间能反应(部分反应物、