题目内容
20.用化学方程式解释生活中的现象,并回答有关问题:(1)湿法冶金的反应原理Fe+CuSO4═FeSO4+Cu.
(2)铁在氧气中燃烧3Fe+2O2$\frac{\underline{\;点燃\;}}{\;}$Fe3O4.
(3)用稀盐酸来除铁锈:Fe2O3+6HCl═2FeCl3+3H2O,反应后溶液的颜色变化为黄色.
(4)用生石灰做干燥剂:CaO+H2O═Ca(OH)2,基本反应类型是化合反应.
分析 首先根据反应原理找出反应物、生成物、反应条件,根据化学方程式的书写方法、步骤(写、配、注、等)进行书写;再根据反应特征确定反应类型.
解答 解:(1)铁和硫酸铜溶液反应生成硫酸亚铁溶液和铜,反应的化学方程式为:Fe+CuSO4═FeSO4+Cu.
(2)铁在氧气中燃烧生成四氧化三铁,反应的化学方程式为3Fe+2O2$\frac{\underline{\;点燃\;}}{\;}$Fe3O4.
(3)铁锈的主要成分是氧化铁,与盐酸反应生成氯化铁和水,反应的化学方程式是:Fe2O3+6HCl═2FeCl3+3H2O.反应后溶液的颜色变化为黄色.
(4)生石灰与水反应生成氢氧化钙,反应的化学方程式为:CaO+H2O═Ca(OH)2;该反应符合“多变一”的特征,属于化合反应.
故答案为:(1)Fe+CuSO4═FeSO4+Cu;(2)3Fe+2O2$\frac{\underline{\;点燃\;}}{\;}$Fe3O4;(3)Fe2O3+6HCl═2FeCl3+3H2O;黄;(4)CaO+H2O═Ca(OH)2;化合反应.
点评 本题难度不大,考查学生根据反应原理书写化学方程式、判定反应类型的能力,掌握化学方程式的书写方法(写、配、注、等)、四种基本反应类型的特征即可正确解答本题.

练习册系列答案
相关题目
7.下列实验设计或结论合理的是( )
| A. | 向某固体滴加稀盐酸,有气泡产生,则该固体一定是碳酸盐 | |
| B. | 除去MgCl2溶液中混有的少量CuCl2,可加入适量的Mg(OH)2,充分搅拌后过滤 | |
| C. | CO32-、Na+、NO3-、K+四种离子可在pH=12的溶液中大量共存 | |
| D. | 将带火星的木条伸入到装有气体的集气瓶中,木条不复燃,证明该气体中不含氧气 |
15.下列成语主要涉及化学变化的是( )
| A. | 刻舟求剑 | B. | 火上浇油 | C. | 花香四溢 | D. | 水落石出 |
5.下列变化属于化学变化的是( )
| A. | 轮胎爆炸 | B. | 灯泡通电发光 | C. | 石油分馏 | D. | 用食醋除水垢 |
12.A、B、C三种物质的溶解度曲线如图所示,下列分析正确的是( )


| A. | t1℃时,A、C两种物质的饱和溶液中溶质的质量相等 | |
| B. | A中混有少量B,可用蒸发结晶的方法提纯A | |
| C. | t2℃时,把50gA放入50g水中能得到A的饱和溶液,其中溶质和溶液的质量比为1:3 | |
| D. | 将t2℃时,A、B、C三种物质的饱和溶液降温至t1℃,所得溶液的溶质质量分数的大小关系是B>C=A |
9.类推是化学学习中常用的思维方法.下列类推结果正确的是( )
| A. | 离子是带电的原子或原子团→带电的粒子就是离子 | |
| B. | 酸碱盐之间的复分解反应一定有盐生成→有盐生成的反应一定是复分解反应 | |
| C. | 点燃H2和O2的混合气体可能爆炸→点燃CH4和O2的混合气体也可能爆炸 | |
| D. | 稀有气体的原子最外电子层一般是8个电子→最外电子层是8个电子的粒子一定是稀有气体的原子 |
10.汽车排放的尾气是造成雾霾天气的主要原因之一.“三效催化转换器”可将汽车尾气中的有毒气体转化为无污染的气体,其中之一的反应微观示意图如图.从图示获得的下列信息错误的是( )
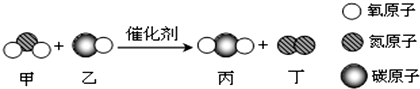

| A. | 分子是化学变化中最小的粒子 | B. | 反应前后共有4种分子 | ||
| C. | 甲和丁中同种元素的化合价不同 | D. | 乙和丙中所含原子种类相同 |