题目内容
16.结合下图回答问题: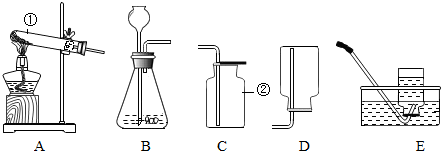
(1)写出指定仪器的名称:①试管,②集气瓶.
(2)实验室用过氧化氢制取氧气时,符号表达式2H2O2$\frac{\underline{\;MnO_2\;}}{\;}$2H2O+O2↑某同学观察到发生装置内有大量气泡时,开始用C装置收集氧气,过一段时间后用带火星的木条伸入瓶口、瓶中和瓶底,都末见木条复燃.其原因是装置漏气.
(3)实验室用高锰酸钾制取氧气,实验结束后,发现水槽内的水变成了紫红色,可能的原因是试管口未放棉花团.
(4)实验室常用醋酸钠固体与碱石灰固体共热来制取甲烷.甲烷常温下是一种无色、无味的气体,密度比空气小.极难溶于水的气体,现选择合适的装置来制取并收集,应该选择的发生装置与收集装置是AD或AE.
(5)实验室用氯酸钾制取氧气时,发现试管破裂,请分析原因(至少两条)没有使用外焰加热、试管外壁有水等.
(6)若用装置C收集氧气如何验满?把带火星的木条放在瓶口,如果木条复燃,则证明该瓶氧气已经收集满了.
(7)求尿素(CO(NH2)2)中氧元素与氮元素的质量比.
分析 (1)要熟悉各种仪器的名称、用途和使用方法;
(2)如果装置漏气,会影响实验结果,甚至会导致实验失败;
(3)根据加热高锰酸钾制取氧气时的实验过程及注意事项分析;
(4)结合装置适用范围与制取甲烷原理综合分析即可;根据甲烷不溶于水及密度小于空气即可分析出收集方法;
(5)据仪器的使用方法和注意事项分析解答;
(6)氧气的验满方法是把带火星的木条放在瓶口来验满,如果带火星的木条在瓶口能复燃,则证明该瓶氧气已经收集满了;
(7)根据化合物中各元素质量比=各原子的相对原子质量×原子个数之比,进行分析解答.
解答 解:(1)①是试管,常用作反应容器;②是集气瓶,常用作收集气体.
故填:试管;集气瓶;
(2)实验室用过氧化氢制取氧气,反应的方程式为:2H2O2$\frac{\underline{\;MnO_2\;}}{\;}$2H2O+O2↑;如果装置漏气,收集的氧气不纯,容易导致带火星的木条不能复燃;
故填:装置漏气;
(3)实验室用高锰酸钾制取氧气,实验结束后,发现水槽内的水变成了紫红色,可能的原因是:试管口未放棉花团.故填:试管口未放棉花团;
(4)通过分析图示装置可知:AB两种装置适用范围不同,A是固体发生装置,B是固液发生装置,此题用醋酸钠和碱石灰共热制取甲烷,发生装置用A,
根据甲烷不溶于水及密度小于空气的特点可知,应用排水法或向下排空气法收集.故选D或E.故填:AD或AE;
(5)加热试管时要进行预热,使用外焰加热,防止试管受热不均引起试管炸裂,其试管外壁不能有水,利用排水法收集时若先熄灯再移导管会造成水倒吸引起试管炸裂等;故填:没有使用外焰加热、试管外壁有水等;
(6)氧气的验满方法是把带火星的木条放在瓶口来验满,如果带火星的木条在瓶口能复燃,则证明该瓶氧气已经收集满了.故填:把带火星的木条放在瓶口,如果木条复燃,则证明该瓶氧气已经收集满了;
(7)尿素中氧、氮、氢元素的质量比为16:(14×2)=4:7.故填:4:7.
点评 据反应物状态和反应条件选择发生装置,据气体密度和溶解性选择收集装置,并掌握反应原理、注意事项等知识,才能结合题意灵活分析解答.

 考前必练系列答案
考前必练系列答案| A. | 浓盐酸 | B. | 浓硫酸 | C. | 无水CuSO4 | D. | 生石灰 |
| A. | 工业上用液态空气制取氧气 | B. | 水通电分解 | ||
| C. | 活性炭吸附水中的色素 | D. | 用过滤方法除去水中杂质 |
| A. | 二氧化氯是氧化物 | B. | 二氧化氯中氯元素的化合价位+4价 | ||
| C. | 二氧化氯由氯元素和氧元素组成 | D. | 二氧化氯分子中含有氧分子 |