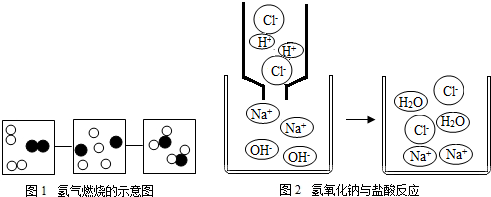
题目内容
14.某学习兴趣小组要用100g质量分数为10%的氢氧化钠溶液来制作“叶脉书签”.如图是他们配制氢氧化钠溶液的操作示意图.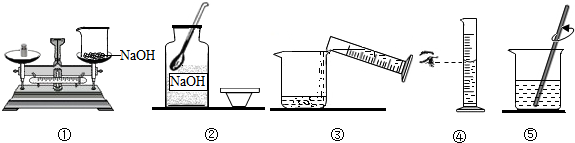
(1)上述操作有错误的是①②(填序号).
(2)操作④选用的量筒是C(填编号,下同).
A.10mL B.50mL C.100mL D.150mL
(3)配制溶液的操作顺序是B.
A.①②③④⑤B.②①④③⑤C.④②①③⑤D.⑤④②①③
(4)在量取水时,若操作④为仰视,则配制的氢氧化钠溶液质量分数偏小(填“偏大”或“偏小”).
(5)配制好的氢氧化钠溶液应密封保存,据你在实验室的观察盛放氢氧化钠溶液的试剂瓶应用胶塞(填“胶塞”或“玻璃瓶盖”).
分析 (1)根据托盘天平的使用要遵循“左物右码”的原则、氢氧化钠具有腐蚀性,固体药品的取用方法进行分析判断.
(2)利用溶质质量=溶液质量×溶质的质量分数,可根据溶液的质量和溶质的质量分数计算配制溶液所需要的溶质的质量;进而溶剂质量=溶液质量-溶质质量,计算出所需水的质量,由所需水的体积判断所需量筒的量程.
(3)根据配制溶质质量分数一定的溶液的基本步骤进行分析解答.
(4)操作④为仰视,读数比实际液体体积大,会造成实际量取的水的体积偏小,据此进行分析解答.
(5)根据氢氧化钠溶液能与玻璃反应,进行分析解答.
解答 解:(1)托盘天平的使用要遵循“左物右码”的原则,图中所示操作砝码与药品位置放反了;取用固体药品时,应用药匙取用,瓶塞要倒放,图中瓶塞没有倒放.
(2)溶质质量=溶液质量×溶质的质量分数,配制100g质量分数为10%的氢氧化钠溶液,需氢氧化钠的质量=100g×10%=10g;溶剂质量=溶液质量-溶质质量,则所需水的质量=100g-10g=90g(合90mL),应选用100mL的量筒.
(3)配制一定质量分数的溶液的步骤:计算、称量(量取)、溶解、装瓶贴签,
(4)操作④为仰视,读数比实际液体体积大,会造成实际量取的水的体积偏小,则配制的氢氧化钠溶液质量分数偏小.
(5)配制好的氢氧化钠溶液应密封保存,氢氧化钠溶液能与玻璃反应,在实验室的观察盛放氢氧化钠溶液的试剂瓶应用胶塞.
故答案为:(1)①②;(2)C;(3)B;(4)偏小;(5)胶塞.
点评 本题难度不大,掌握配制溶质质量分数一定的溶液的基本步骤、注意事项等是正确解答本题的关键.

练习册系列答案
 每日10分钟口算心算速算天天练系列答案
每日10分钟口算心算速算天天练系列答案
相关题目
4. 为验证混合气体中是否含有CO,CO2,H2O,H2 这四种气体,现有无水硫酸铜,澄清石灰水,浓硫酸,氢氧化钠溶液以及如图所示装置甲.能验证这四种气体的方法正确的是( )
为验证混合气体中是否含有CO,CO2,H2O,H2 这四种气体,现有无水硫酸铜,澄清石灰水,浓硫酸,氢氧化钠溶液以及如图所示装置甲.能验证这四种气体的方法正确的是( )
 为验证混合气体中是否含有CO,CO2,H2O,H2 这四种气体,现有无水硫酸铜,澄清石灰水,浓硫酸,氢氧化钠溶液以及如图所示装置甲.能验证这四种气体的方法正确的是( )
为验证混合气体中是否含有CO,CO2,H2O,H2 这四种气体,现有无水硫酸铜,澄清石灰水,浓硫酸,氢氧化钠溶液以及如图所示装置甲.能验证这四种气体的方法正确的是( )| A. | 依次通入无水硫酸铜,澄清石灰水,浓硫酸,甲装置,无水硫酸铜,澄清石灰水 | |
| B. | 依次通入无水硫酸铜,澄清石灰水,甲装置,无水硫酸铜,澄清石灰水 | |
| C. | 依次通入澄清石灰水,无水硫酸铜,浓硫酸,甲装置,无水硫酸铜,澄清石灰水 | |
| D. | 依次通入无水硫酸铜,澄清石灰水,浓硫酸,甲装置,澄清石灰水,无水硫酸铜 |
5.现有KCl、NaCl、Na2CO3组成的混合物,该混合物中Na+的质量分数为31.5%,Cl-的质量分数为27.08%.则混合物中Na2CO3的质量分数为( )
| A. | 40% | B. | 60% | C. | 50% | D. | 30% |
2.下列物质的用途主要是由其化学性质决定的是( )
| A. | 用干冰做制冷剂 | B. | 用金刚石切割玻璃 | ||
| C. | 用天然气作燃料 | D. | 发烧病人用酒精擦身体降温 |
9. 元素周期表是学习化学的重要工具.如表是元素周期表的一部分,请依据此表回答有关问题.
元素周期表是学习化学的重要工具.如表是元素周期表的一部分,请依据此表回答有关问题.
(1)第二周期中,氮元素的相对原子质量为14.01.第三周期中,原子结构属于稳定结构的元素是氩(填元素名称).
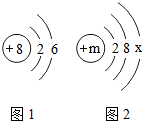
(2)氧元素的原子结构示意图如图1,第3周期中某元素与氧元素的化学性质相似,该元素的原子结构示意图为如图2,则m=16,x=6.
(3)从原子序数分别为1、8、11、12、17的五种元素中,选择适当的元素组成物质,则这些物质之间能发生复分解反应的化学方程式为(只写一个)HCl+NaOH=NaCl+H2O.
 元素周期表是学习化学的重要工具.如表是元素周期表的一部分,请依据此表回答有关问题.
元素周期表是学习化学的重要工具.如表是元素周期表的一部分,请依据此表回答有关问题.| 第一周期 | 1 H 1.008 | 2 He 4.003 | ||||||
| 第二周期 | 3 Li 6.941 | 4 Be 9.012 | 5 B 10.81 | 6 C 12.01 | 7 N 14.01 | 8 O 16.00 | 9 F 19.00 | 10 Ne 20.18 |
| 第三周期 | 11 Na 22.99 | 12 Mg 24.31 | 13 Al 26.98 | 14 Si 28.09 | 15 P 30.97 | 16 S 32.06 | 17 Cl 35.45 | 18 Ar 39.95 |
(2)氧元素的原子结构示意图如图1,第3周期中某元素与氧元素的化学性质相似,该元素的原子结构示意图为如图2,则m=16,x=6.
(3)从原子序数分别为1、8、11、12、17的五种元素中,选择适当的元素组成物质,则这些物质之间能发生复分解反应的化学方程式为(只写一个)HCl+NaOH=NaCl+H2O.
19.我国科学家用滤纸和二氧化钛(TiO2)薄膜制作出一种新型“纳米纸”,又在纳米纸上“铺”一层“萘胺”(C10H9N)染料,制成一种试纸,用于检测食品中亚硝酸盐浓度的高低.相关的下列说法中,正确的是( )
| A. | 不同浓度的亚硝酸盐会使萘胺显不同颜色 | |
| B. | 二氧化钛中Ti的化合价为+2 | |
| C. | 萘胺的相对分子质量为143克 | |
| D. | 这种试纸是一种新型化合物 |
3. 如下猜想:可能部分变质,固体是NaOH和 Na2CO3的混合物;可能全部变质,固体是Na2CO3.
如下猜想:可能部分变质,固体是NaOH和 Na2CO3的混合物;可能全部变质,固体是Na2CO3.
(1)首先对固体的成分进行确定.取少量固体于试管中,加水充分溶解,先加入足量的BaCl2 溶液,产生白色沉淀,静置后取上层清液,再加入CuSO4 溶液,产生蓝色絮状沉淀.根据实验现象,可确定该固体是NaOH和Na2CO3 的混合物;
(2)称取10.6g 该固体样品于锥形瓶中,加入一定质量分数的稀盐酸,直至过量,得到数据如表:
计算该样品中Na2CO3的质量分数.
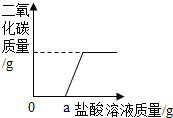
(3)再取固体样品溶于水,加入一定质量分数的稀盐酸,直至过量.测出加入稀盐酸的质量与产生CO2气体的质量关系如图所示.从图中可以判断:在该样品溶液中加入稀盐酸,首先与之反应的物质是NaOH.
(4)请你分析,一定质量的NaOH固体,变质前后与相同质量分数的稀盐酸反应,变质前消耗盐酸的量等于变质后消耗盐酸的量(填“大于”、“小于”或“等于”).
 如下猜想:可能部分变质,固体是NaOH和 Na2CO3的混合物;可能全部变质,固体是Na2CO3.
如下猜想:可能部分变质,固体是NaOH和 Na2CO3的混合物;可能全部变质,固体是Na2CO3.(1)首先对固体的成分进行确定.取少量固体于试管中,加水充分溶解,先加入足量的BaCl2 溶液,产生白色沉淀,静置后取上层清液,再加入CuSO4 溶液,产生蓝色絮状沉淀.根据实验现象,可确定该固体是NaOH和Na2CO3 的混合物;
(2)称取10.6g 该固体样品于锥形瓶中,加入一定质量分数的稀盐酸,直至过量,得到数据如表:
| 样品质量 | 反应前总质量 | 反应后总质量 |
| 10.6克 | 148.5克 | 146.3克 |
(3)再取固体样品溶于水,加入一定质量分数的稀盐酸,直至过量.测出加入稀盐酸的质量与产生CO2气体的质量关系如图所示.从图中可以判断:在该样品溶液中加入稀盐酸,首先与之反应的物质是NaOH.
(4)请你分析,一定质量的NaOH固体,变质前后与相同质量分数的稀盐酸反应,变质前消耗盐酸的量等于变质后消耗盐酸的量(填“大于”、“小于”或“等于”).
4.下列做法正确的是( )
| A. | 用聚氯乙烯塑料包装食品袋可以用加热挤压的方法封口 | |
| B. | 扑灭汽油、柴油燃烧引起的失火既可用干粉灭火器又可用水基型灭火器 | |
| C. | 烧煤时,把大块煤砸成小块,使煤燃烧更充分,以减少二氧化硫和一氧化碳的排放 | |
| D. | 用盐酸除铁制器皿的水垢时,应浸泡足够长的时间 |