题目内容
6.雨欣同学设计了如图实验装置验证一氧化碳的部分性质并验证产物.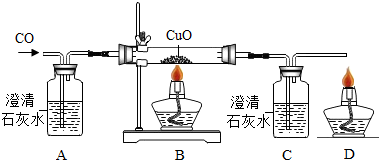
(1)实验时,在点燃B处酒精灯之前先通一段时间一氧化碳的目的是把玻璃管中空气全部排出,实验过程中B处玻璃管中的现象是黑色粉末变红.
(2)C中反应的化学方程式是Ca(OH)2+CO2═CaCO3↓+H2O,D处点燃的目的是防止有毒的一氧化碳排放到空气中污染环境.
(3)对该实验的分析正确的是C(填序号);
①实验结束时应先熄灭D处酒精灯
②C中增加的质量与B中固体减小的质量相等
③反应结束后,若生成了6.4g的铜,则通入的一氧化碳质量一定大于2.8g
(4)雨欣同学认为A装置用于证明一氧化碳不能和石灰水反应,有同学认为省略A可达到同样的目的,理由是为了排尽装置内的空气,反应前已经通入一段时间的CO.
分析 根据已有的一氧化碳还原氧化铜的知识进行分析解答,一氧化碳能与氧化铜反应生成铜和二氧化碳,其中一氧化碳具有还原性;一氧化碳是有毒的气体,需要进行尾气处理,根据一氧化碳和氧化铜反应的注意事项以及物质的质量的关系进行解答即可.
解答 解:(1)由于CO气体与空气混合在加热时可能出现爆炸,因此,在进行加热前要把玻璃管中空气全部排出,所以进行操作时应先通入CO排出管内空气然后再进行加热;一氧化碳和氧化铜在加热时生成铜和二氧化碳,会观察到会黑色粉末变红;
(2)C中二氧化碳能使澄清的石灰水变浑浊,故其化学方程式为Ca(OH)2+CO2═CaCO3↓+H2O;一氧化碳是有毒的气体,点燃能防止有毒的一氧化碳排放到空气中污染环境;
(3)A、实验结束时应先熄灭B处酒精灯,故A错误;
B、C中增加的质量是二氧化碳的质量,B中固体减小的质量是氧元素的质量,故质量不相等,故B错误;
C、该反应前后都要通入一氧化碳,所以若生成了6.4g的铜,则通入的一氧化碳质量一定大于2.8g,故C正确;故选:C;
(4)省略A可达到同样的目的,因为为了排尽装置内的空气,反应前已经通入一段时间的CO,故填:为了排尽装置内的空气,反应前已经通入一段时间的CO.
故答案为:
(1)把玻璃管中空气全部排出,黑色粉末变红.
(2)Ca(OH)2+CO2═CaCO3↓+H2O,防止有毒的一氧化碳排放到空气中污染环境.
(3)C;(4)为了排尽装置内的空气,反应前已经通入一段时间的CO.
点评 本题考查的是一氧化碳还原氧化铜的知识,完成此题,可以依据已有的知识结合物质的性质进行.

练习册系列答案
相关题目
15.植物进行光合作用可表示为:水+二氧化碳 $→_{叶绿素}^{光}$ 淀粉+氧气,据此可知淀粉的组成一定含有的元素是( )
| A. | 碳、氢和氧 | B. | 碳、氧 | C. | 氢、氧 | D. | 碳、氢 |
14.下列物质燃烧的现象描述,正确的是( )
| A. | 硫在氧气中燃烧发出淡蓝色火焰,放热,生成有刺激性气味的气体 | |
| B. | 木炭在氧气中燃烧生成一种能使澄清石灰水变浑浊的气体二氧化碳 | |
| C. | 镁条在空气中燃烧,发出耀眼的白光,生成一种白色固体 | |
| D. | 红磷在空气中燃烧,产生大量白雾 |
11.如图所示是利用海水提取粗盐的过程:

根据海水晒盐的原理,下列说法中:①海水进入贮水池,海水的成分基本不变②在蒸发池中,海水中氯化钠的质量逐渐增加③在蒸发池中,海水中水的质量逐渐增加④析出晶体后的母液是氯化钠的饱和溶液,正确的是( )

根据海水晒盐的原理,下列说法中:①海水进入贮水池,海水的成分基本不变②在蒸发池中,海水中氯化钠的质量逐渐增加③在蒸发池中,海水中水的质量逐渐增加④析出晶体后的母液是氯化钠的饱和溶液,正确的是( )
| A. | ①③ | B. | ②④ | C. | ①④ | D. | ②③ |
18.规范的实验操作时实验成功的保证,下列实验操作或设计错误的是( )
| A. |  取用固体 | B. | 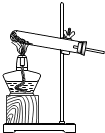 加热固体 | ||
| C. | 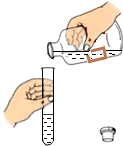 取用液体 取用液体 | D. | 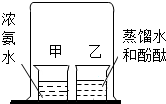 探究分子的运动 |
16.我国科学家屠呦呦因为“发现青蒿素(化学式为C15H22O5),一种用于治疗疟疾的药物,挽救了全球特别是发展中国家的数百万人的生命”而获诺贝尔奖,下列关于青蒿素的说法不正确的是( )
| A. | 一个青蒿素分子中含有42个原子 | |
| B. | 青蒿素的相对分子质量为282 | |
| C. | 青蒿素中C、H、O三种元素的质量比为90:11:40 | |
| D. | 青蒿素中碳元素质量分数为28.4% |
