题目内容
12.有Fe和另一种金属组成的混合物4.5克,与足量的盐酸反应,产生氢气的质量是0.2克,则另一种金属可能是( )| A. | Ag | B. | Zn | C. | Mg | D. | Cu |
分析 稀盐酸和铁、锌、镁反应生成盐和氢气,不能和银、铜反应.
解答 解:稀盐酸和铁、锌、镁反应生成盐和氢气,反应的化学方程式及其质量关系为:
Fe+2HCl═FeCl2+H2↑,
56 2
Zn+2HCl═ZnCl2+H2↑,
65 2
Mg+2HCl═MgCl2+H2↑,
24 2
由以上质量关系可知,4.5g铁、锌和足量稀盐酸反应时生成氢气的质量都小于0.2g,4.5g镁和稀盐酸反应生成氢气质量大于0.2g,因此与足量的盐酸反应时产生氢气的质量是0.2g,则另一种金属可能是镁.
故选:C.
点评 本题主要考查物质的性质,解答时要根据各种物质的性质,结合各方面条件进行分析、判断,从而得出正确的结论.

练习册系列答案
 捷径训练检测卷系列答案
捷径训练检测卷系列答案 小夫子全能检测系列答案
小夫子全能检测系列答案
相关题目
2.某实验小组对实验室中A、B、C、D四瓶无色溶液进行鉴别,它们分别是硫酸钠、稀硫酸、澄清石灰水、氯化钙四种物质的一种.可供使用的实验用品有:稀盐酸、稀硫酸、碳酸钠、紫色石蕊溶液、硝酸钡溶液、硝酸银溶液、稀硝酸溶液、玻璃棒、试管、胶头滴管.请利用提供的实验用品,鉴别出四种物质,并完成实验报告:
| 实验 | 实验操作 | 实验现象 | 实验结论 |
| ① | 取四支试管,各取少量的A、B、C、D溶液,分别先滴加紫色石蕊试液 | B溶液变红色,D溶液变成蓝色.A、C溶液都呈紫色. | B是稀硫酸 D是澄清的石灰水 |
| ② | 另取二支试管,各取少量的A、C溶液,分别先滴入硝酸钡溶液后再滴入稀硝酸溶液. | A溶液中产生白色沉淀、 C溶液无明显变化 | A是硫酸钠溶液 C是氯化钙溶液 |
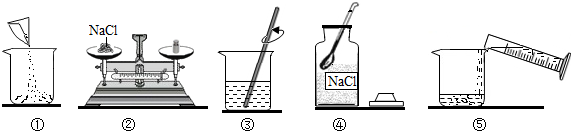
3.下图所示操作中,正确的是( )
| A. | 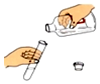 取用液体 | B. | 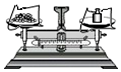 称量氯化钠固体 | ||
| C. | 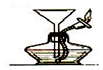 向酒精灯内添加酒精 | D. | 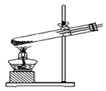 加热固体 |
7.下列物质长期暴露在空气中容易变质的是( )
| A. | 氢氧化钠 | B. | 食盐 | C. | 食醋 | D. | 硫酸 |
17.将等质量的镁、铁、锌,分别放入三份足量的稀盐酸中,反应生成的H2质量最多的是( )
| A. | 镁 | B. | 铁 | C. | 锌 | D. | 一样多 |
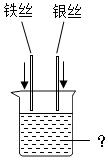 小燕同学设计了如图所示的实验来验证金属的活动性顺序.请回答:
小燕同学设计了如图所示的实验来验证金属的活动性顺序.请回答: