题目内容
元素周期表是我们学习和研究化学的重要工具,通过元素周期表我们能获得许多信息,如表是元素周期表的一部分,根据图表回答下列问题:
(1)氟元素的相对原子质量是 ,氟属于 元素(填“金属”或“非金属”);
(2)写出原子序数为13、17二种元素所组成的化合物的化学式: .
(3)科学家宣布已人工合成了第120号元素,则此元素的核电荷数为 .
(4)表中与P元素化学性质相似的元素是 .
(5)铝原子在化学反应中容易 (填“得到”或“失去”)形成 离子(填“阳”或“阳”).
| 1H 1.008 | 2He 4.003 | ||||||
| 3Li 6.941 | 4Be 9.012 | 5B 10.81 | 6C 12.01 | 7N 14.01 | 8O 16.00 | 9F 19.00 | 10Ne 20.18 |
| 11Na 22.99 | 12Mg 24.31 | 13Al 26.98 | 14Si 28.09 | 15P 30.97 | 16S 32.06 | 17Cl 35.45 | 18Ar 39.95 |
(2)写出原子序数为13、17二种元素所组成的化合物的化学式:
(3)科学家宣布已人工合成了第120号元素,则此元素的核电荷数为
(4)表中与P元素化学性质相似的元素是
(5)铝原子在化学反应中容易
考点:元素周期表的特点及其应用,元素的简单分类,化学式的书写及意义
专题:化学用语和质量守恒定律
分析:(1)根据图中元素周期表可以获得的信息:左上角的数字表示原子序数;字母表示该元素的元素符号;中间的汉字表示元素名称;汉字下面的数字表示相对原子质量,进行分析解答即可.
(2)原子序数为13、17二种元素分别是铝元素、氯元素,据此进行分析解答.
(3)根据在原子中,原子序数=核电荷数,进行分析解答.
(4)根据同一族的元素具有相似的化学性质,进行分析判断.
(5)铝原子的原子序数为13,根据原子序数=核电荷数=质子数=核外电子数,则该元素的原子核外电子数为13,第一层上有2个电子,第二层上有8个电子,最外层电子数为3,据此进行分析解答.
(2)原子序数为13、17二种元素分别是铝元素、氯元素,据此进行分析解答.
(3)根据在原子中,原子序数=核电荷数,进行分析解答.
(4)根据同一族的元素具有相似的化学性质,进行分析判断.
(5)铝原子的原子序数为13,根据原子序数=核电荷数=质子数=核外电子数,则该元素的原子核外电子数为13,第一层上有2个电子,第二层上有8个电子,最外层电子数为3,据此进行分析解答.
解答:解:(1)根据元素周期表中的一格中获取的信息,可知氟元素的相对原子质量为19.00;氟带“气”字旁,属于非金属元素.
(2)原子序数为13、17二种元素分别是铝元素、氯元素,铝元素显+3价,氯元素显-1价,所组成的化合物为氯化铝,其化学式为AlCl3.
(3)在原子中,原子序数=核电荷数,120号元素的原子序数为120,故此元素的核电荷数为120.
(4)同一族的元素具有相似的化学性质,表中氮元素与P元素位于同一族,化学性质相似.
(5)铝原子的原子序数为13,根据原子序数=核电荷数=质子数=核外电子数,则该元素的原子核外电子数为13,第一层上有2个电子,第二层上有8个电子,最外层电子数为3,在化学反应中易失去3个电子而形成阳离子.
故答案为:(1)19.00;非金属;(2)AlCl3;(3)120;(4)氮;(5)失去;阳.
(2)原子序数为13、17二种元素分别是铝元素、氯元素,铝元素显+3价,氯元素显-1价,所组成的化合物为氯化铝,其化学式为AlCl3.
(3)在原子中,原子序数=核电荷数,120号元素的原子序数为120,故此元素的核电荷数为120.
(4)同一族的元素具有相似的化学性质,表中氮元素与P元素位于同一族,化学性质相似.
(5)铝原子的原子序数为13,根据原子序数=核电荷数=质子数=核外电子数,则该元素的原子核外电子数为13,第一层上有2个电子,第二层上有8个电子,最外层电子数为3,在化学反应中易失去3个电子而形成阳离子.
故答案为:(1)19.00;非金属;(2)AlCl3;(3)120;(4)氮;(5)失去;阳.
点评:本题难度不大,灵活运用元素周期表中元素的信息并能灵活运用是正确解答本题的关键.

练习册系列答案
 学练快车道快乐假期暑假作业新疆人民出版社系列答案
学练快车道快乐假期暑假作业新疆人民出版社系列答案 浙大优学小学年级衔接导与练浙江大学出版社系列答案
浙大优学小学年级衔接导与练浙江大学出版社系列答案 小学暑假作业东南大学出版社系列答案
小学暑假作业东南大学出版社系列答案
相关题目
下列有关的叙述正确的是( )
| A、某物质不是化合物就是单质 |
| B、化合物不一定是纯净物 |
| C、O2和O3相互转变是物理变化 |
| D、混合物中的元素不一定存在于单质中 |
下列实验现象的描述中,正确的是( )
| A、硫在空气中燃烧发出明亮的蓝紫色火焰 |
| B、将盛有饱和石灰水的试管放入热水中,石灰水变浑浊 |
| C、分别点燃一小块腈纶纤维和羊毛纤维,都产生了烧焦羽毛味 |
| D、将硫酸铵和熟石灰混合研磨,生成无色无味的气体 |
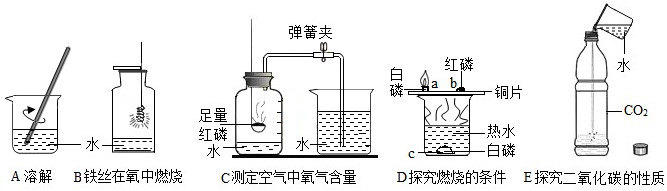
 如图1所示的是电解水实验装置.通电一段时间后,在两个试管中分别收集到气体a和气体b.请回答:
如图1所示的是电解水实验装置.通电一段时间后,在两个试管中分别收集到气体a和气体b.请回答: 某化学兴趣小组查阅资料得知:过氧化钠(Na2O2)是一种黄色粉末,常温下能与二氧化碳反应产生氧气,常用在潜水艇中作供氧剂.该小组同学将过氧化钠与二氧化碳反应后,发现除了生成氧气,还生成了一种白色固体.
某化学兴趣小组查阅资料得知:过氧化钠(Na2O2)是一种黄色粉末,常温下能与二氧化碳反应产生氧气,常用在潜水艇中作供氧剂.该小组同学将过氧化钠与二氧化碳反应后,发现除了生成氧气,还生成了一种白色固体. 化学基本观念是化学基本思想和方法在头脑中的综合与提升,是我们化学学习的最终结果和对化学认识的最高境界.现以水的知识为基础,帮助你构建化学观.
化学基本观念是化学基本思想和方法在头脑中的综合与提升,是我们化学学习的最终结果和对化学认识的最高境界.现以水的知识为基础,帮助你构建化学观. ”表示水分子,请用图示表示水通电分解的变化过程:
”表示水分子,请用图示表示水通电分解的变化过程:
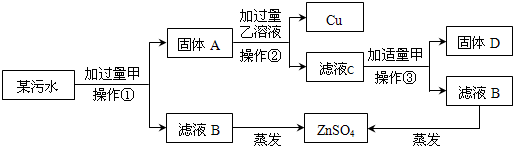
 A、B、C、D、E是初中化学中常见的不同类别的物质(物质按单质、氧化物、酸、碱、盐分类).已知A是单质,C是红棕色固体;E是一种盐,E的水溶液可使酚酞试液变为红色.图中“-”表示相连的物质两两之间可以发生反应,“→”表示由某一物质可制得另一物质(部分反应物、生成物及反应条件已略去).回答下列问题:
A、B、C、D、E是初中化学中常见的不同类别的物质(物质按单质、氧化物、酸、碱、盐分类).已知A是单质,C是红棕色固体;E是一种盐,E的水溶液可使酚酞试液变为红色.图中“-”表示相连的物质两两之间可以发生反应,“→”表示由某一物质可制得另一物质(部分反应物、生成物及反应条件已略去).回答下列问题: