题目内容
1.下列实验方法、现象、结论均正确的是( )| 选项 | 实验方法 | 现象 | 结论 |
| A | 用pH试纸测肥皂液的酸碱性 | 试纸变蓝(pH>7) | 肥皂液呈碱性 |
| B | 铜丝放入稀硝酸中 | 有气泡产生 | 铜可以置换出酸中的氢气 |
| C | 燃烧法测定纤维种类 | 烧毛发的气味 | 该纤维是棉纤维 |
| D | 向醋酸中加入氢氧化钠溶液 | 无明显现象 | 二者之间不发生反应 |
| A. | A | B. | B | C. | C | D. | D |
分析 A、根据肥皂液显碱性解答;
B、根据硝酸具有强的氧化性,铜与足量的硝酸反应生成产物为:硝酸铜、一氧化氮、水解答;
C、根据烧毛发的气味,主要成分是蛋白质解答;
D、根据酸和碱发生中和反应解答.
解答 解:
A、用pH试纸测肥皂液的酸碱性,试纸变黄(pH>7),肥皂液显碱性,故对;
B、硝酸具有强的氧化性,铜与足量的硝酸反应生成产物为:硝酸铜、一氧化氮、水,不是铜可以置换出酸中的氢气,故错;
C、烧毛发的气味,主要成分是蛋白质,棉纤维无蛋白质,故错;
D、向醋酸中加入氢氧化钠溶液,酸和碱发生中和反应,无现象,故错.
答案:A.
点评 本题考查较为综合,侧重于学生的分析能力和实验能力的考查,注意相关基础知识的积累,难度不大.

练习册系列答案
相关题目
11.化学是一门以实验为基础的科学,许多化学重大发现和研究成果都是通过实验得到的.下列实验操作或设计中正确的是( )
| A. | 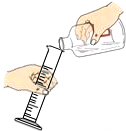 用100mL量筒量取8.5mL盐酸 | B. | 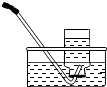 收集氧气 | ||
| C. | 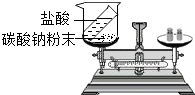 验证质量守恒定律 | D. | 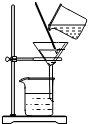 分离碘酒中的碘 |
9.下列事故处理方法不正确的是( )
| A. | 电器着火,立即用水扑灭 | |
| B. | 图书馆内图书着火,立即用液态CO2扑灭 | |
| C. | 厨房煤气管道漏气,立即关闭阀门并开窗通风 | |
| D. | 炒菜时油锅着火,立即盖上锅盖 |
6.有一包白色粉末,可能含有Ba(OH)2、KNO3、Na2CO3、Na2SO4中的一种或几种.为了确定其成分,进行如下实验:①取一定量的白色粉末加入足量的水,振荡,静置,得白色沉淀,上层清液为无色.②过滤,在白色沉淀中加入足量稀盐酸,白色沉淀全部溶解,且有气泡产生.下列对白色粉末成分的判断中,不正确的是( )
| A. | 一定有Na2CO3 | B. | 可能有Na2SO4 | C. | 一定有Ba(OH)2 | D. | 可能有KNO3 |
13.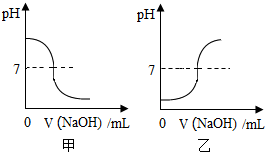 NaOH是化学实验中常用的试剂.
NaOH是化学实验中常用的试剂.
(1)将某NaOH溶液逐滴滴入一定量的某盐酸中,右边图象合理的是乙(填“甲”或“乙”).
(2)向长期敞口放置的NaOH固体中滴加盐酸时,小丽意外发现有气泡
产生,她认为氢氧化钠已经变质了.用化学方程式表示氢氧化钠变质的原因:2NaOH+CO2=Na2CO3+H2O.
【提出问题】氢氧化钠变质后的成分及程度?
【猜想假设】小丽对变质后的氢氧化钠样品的成分做出了两种猜想:
猜想一:NaOH、Na2CO3;猜想二:Na2CO3.
【实验设计】为验证上述猜想哪个正确,小丽设计了如下方案:取少量氢氧化钠样品于试管中加水溶解,滴加几滴无色酚酞溶液,观察溶液颜色变化.小红认为小丽的实验方案不合理,理由是:氢氧化钠和碳酸钠的水溶液都呈碱性,都能使无色酚酞溶液变红(表述合理即可).
【实验与结论】小红另外设计并完成了实验,请你帮她填写下面的实验报告:
上述步骤1中,滴加过量氯化钙溶液的目的是除去碳酸钠,防止对氢氧化钠的碱性检验产生干扰
【拓展应用】①为测定出该NaOH固体的变质程度,继续将上述白色沉淀过滤、洗净、干燥,称得其质量为2g,则固体样品中NaOH的质量分数为73.5%(假定试剂中无其它杂质).
②要除去氢氧化钠中含有的碳酸钠,所用的方法(用化学方程式表示)Na2CO3+Ca(OH)2═CaCO3↓+2NaOH.
 NaOH是化学实验中常用的试剂.
NaOH是化学实验中常用的试剂.(1)将某NaOH溶液逐滴滴入一定量的某盐酸中,右边图象合理的是乙(填“甲”或“乙”).
(2)向长期敞口放置的NaOH固体中滴加盐酸时,小丽意外发现有气泡
产生,她认为氢氧化钠已经变质了.用化学方程式表示氢氧化钠变质的原因:2NaOH+CO2=Na2CO3+H2O.
【提出问题】氢氧化钠变质后的成分及程度?
【猜想假设】小丽对变质后的氢氧化钠样品的成分做出了两种猜想:
猜想一:NaOH、Na2CO3;猜想二:Na2CO3.
【实验设计】为验证上述猜想哪个正确,小丽设计了如下方案:取少量氢氧化钠样品于试管中加水溶解,滴加几滴无色酚酞溶液,观察溶液颜色变化.小红认为小丽的实验方案不合理,理由是:氢氧化钠和碳酸钠的水溶液都呈碱性,都能使无色酚酞溶液变红(表述合理即可).
【实验与结论】小红另外设计并完成了实验,请你帮她填写下面的实验报告:
| 实验步骤 | 实验现象 | 结论 |
| 步骤1:称取上述固体样品8g溶于100mL水配成溶液, 向溶液中滴加过量的氯化钙溶液充分反应后,静置. | 有白色沉淀产生 | 猜想一 正确 |
| 步骤2:将步骤1试管中的混合物过滤,向滤液中滴加无色酚酞溶液 | 溶液变成红色 |
【拓展应用】①为测定出该NaOH固体的变质程度,继续将上述白色沉淀过滤、洗净、干燥,称得其质量为2g,则固体样品中NaOH的质量分数为73.5%(假定试剂中无其它杂质).
②要除去氢氧化钠中含有的碳酸钠,所用的方法(用化学方程式表示)Na2CO3+Ca(OH)2═CaCO3↓+2NaOH.
10.下列各组物质按单质、化合物、混合物顺序排列的是( )
| A. | 冰、生石灰、天然气 | B. | 金刚石、烧碱、食盐水 | ||
| C. | 碘酒、纯碱、胆矾 | D. | 液态氧、盐酸、沼气 |
 某校化学兴趣小组为了测定某一碳酸钠样品中碳酸钠的质量分数,进行如下实验,取13.25g碳酸钠样品(杂质既不溶于酸也不溶于水)放入烧杯中,加入95.8g水使其完全溶解,再向其中加入稀硫酸,测得反应放出气体的总质量与所加入稀硫酸的质量关系曲线如图所示,请根据题意解答问题:
某校化学兴趣小组为了测定某一碳酸钠样品中碳酸钠的质量分数,进行如下实验,取13.25g碳酸钠样品(杂质既不溶于酸也不溶于水)放入烧杯中,加入95.8g水使其完全溶解,再向其中加入稀硫酸,测得反应放出气体的总质量与所加入稀硫酸的质量关系曲线如图所示,请根据题意解答问题:
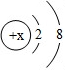 ,它与氯元素组成的离子化合物的化学式为RCl2,则元素R氧化物的化学式为RO.
,它与氯元素组成的离子化合物的化学式为RCl2,则元素R氧化物的化学式为RO.