题目内容
6.图1是A、B、C是微粒的结构示意图,图2是两种元素在元素周期表的信息.
(1)图1中A结构示意图中x=8;C结构示意图中y=8;B结构示意图是阴离子的结构示意图(填“原子”、“阳离子”、“阴离子”).
(2)图2中方框内的横线上应填的元素符号是F;图1中B结构示意图的化学符号为Cl-.
(3)图1中三种结构示意图表示的微粒,两两结合形成的物质的化学式为Na2O.
分析 (1)在原子中,核内质子数等于等于核外电子数;根据核外电子排布的特点,第二层排满时排8个电子;(2)由元素在周期表中的相关信息可知,方框内的横线上应填氟元素的符号,由图1中B结构示意图的可知,核内质子数是17的元素是氯元素,可以写出微粒的符号;
(3)根据它们得失电子情况,判断其组成的化合物的化学式.
解答 解:(1)在原子中,核内质子数等于等于核外电子数,图1中A结构示意图中x=2+6=8,第二层排满时排8个电子,B结构示意图质子数小于电子数,是阴离子结构示意图;
(2)由元素在周期表中的相关信息可知,方框内的横线上应填氟元素的符号:F,由图1中B结构示意图的可知,核内质子数是17的元素是氯元素,该微粒为氯离子,符号为:Cl-;
(3)由图1中结构示意图表示的微粒可以看出,A为氧原子,B粒子为氯离子,C粒子为钠原子,氧原子能与钠原子结合形成的化合物的化学是为:Na2O.
故答为:(1)8;8;阴离子;(2)F,Cl-,阴离子;(3)Na2O.
点评 了解原子结构示意图与离子结构示意图的区别和联系;掌握核外电子在化学变化中的作用和得失电子的规律特点;了解元素周期表的特点及其应用.

练习册系列答案
相关题目
4.配制40g 5%的氯化钠溶液时,不需要用到的仪器是( )
| A. | 托盘天平 | B. | 量筒 | C. | 烧杯 | D. | 漏斗 |
17.下列过程中只发生物理变化的是( )
| A. | 水通电分解 | B. | 冰雪消融 | C. | 钢铁生锈 | D. | 植物光合作用 |
1.下列关于质量守恒定律的说法正确的是( )
| A. | 5g酒精溶解于55克水中形成60克溶液,这符合质量守恒定律 | |
| B. | 2L氢气和1L氧气点燃后生成了3L水 | |
| C. | 15克硫磺在30克氧气中充分燃烧生成45克二氧化碳 | |
| D. | 木材隔绝空气加强热变成木炭后质量减轻,这符合质量守恒定律 |
11.如图所示实驗操作中正确的是( )
| A. |  | B. |  | C. |  | D. |  |
15.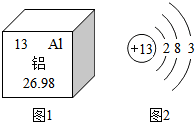 如图1是铝元素的部分信息,图2是铝原子的结构示意图.下列说法不正确的是( )
如图1是铝元素的部分信息,图2是铝原子的结构示意图.下列说法不正确的是( )
 如图1是铝元素的部分信息,图2是铝原子的结构示意图.下列说法不正确的是( )
如图1是铝元素的部分信息,图2是铝原子的结构示意图.下列说法不正确的是( )| A. | 铝元素原子核内的质子数为13 | B. | 铝的相对原子质量为26.98g | ||
| C. | 铝原子的核外电子分三层排布 | D. | 铝原子在化学变化中容易失去电子 |
16.我们在做“物质的鉴别”实验时,曾对硫酸铜、氯化钠、硝酸钾、氢氧化钠四种白色粉末进行鉴别.以下是某同学设计的鉴别方案,请你沿着该同学的思路回答相关问题.
| 步骤 | 现象 | 结论 | |
| (1) | 各取少量白色粉末于试管中,分别编号为A、B、C、D,各加入少量的水,振荡 | D试管溶液呈蓝色 | D物质是硫酸铜 |
| (2) | 向另三支试管内各滴一滴无色酚酞 | A试管溶液呈红色 | A物质是氢氧化钠 |
| (3) | 向B、C两支试管内各滴加少量的硝酸银溶液 | B试管无现象,C试管产生白色沉淀 | B物质是硝酸钾 C物质是氯化钠 |
 、
、 、
、 、
、 分别表示四中含有不同质子数的原子,根据图示回答:
分别表示四中含有不同质子数的原子,根据图示回答:
 =2:1;(用微观示意图表示参加反应的反应物)
=2:1;(用微观示意图表示参加反应的反应物) ”图表示参加反应的反应物构成的物质不一定(填“一定”、“不一定”或“一定不”)是该反应的催化剂;
”图表示参加反应的反应物构成的物质不一定(填“一定”、“不一定”或“一定不”)是该反应的催化剂; ②
② ③
③ ④
④ ⑤
⑤ ⑥
⑥ ⑦
⑦ ⑧
⑧