题目内容
 帕拉米韦注射液可用于治疗H7N9禽流感,其说明书中部分内容如图.
帕拉米韦注射液可用于治疗H7N9禽流感,其说明书中部分内容如图.(1)帕拉米韦由
(2)帕拉米韦中氢、氮、氧、碳四种元素的质量比为
(3)成人禽流感患者,每天应注射帕拉米韦
考点:化学式的书写及意义,元素质量比的计算
专题:化学用语和质量守恒定律
分析:(1)根据化学式的意义进行分析判断.
(2)根据化合物中各元素质量比=各原子的相对原子质量×原子个数之比,进行分析解答;
(3)若每支注射液中帕拉米韦的含量为25mg/支,成人用量为75mg/次,2次/日,据此进行分析解答.
(2)根据化合物中各元素质量比=各原子的相对原子质量×原子个数之比,进行分析解答;
(3)若每支注射液中帕拉米韦的含量为25mg/支,成人用量为75mg/次,2次/日,据此进行分析解答.
解答:解:
(1)由帕拉米韦的化学式可知,它是由碳、氢、氧、氮四种元素组成的,其中氢、氮的原子个数比为28:4=7:1;
(2)帕拉米韦中C、H、N、O元素质量比为(12×15):(1×28):(14×4):(16×4)=45:7:14:16;
(3)每支注射液中帕拉米韦的含量为25mg/支,成人用量为75mg/次,2次/日,则成人每日需注射量为75mg/次×2次=150mg,则每天应注射帕拉米韦注射液150mg÷25mg/支=6支;
故答案为:
(1)4;7:1;
(2)45:7:14:16;
(3)6.
(1)由帕拉米韦的化学式可知,它是由碳、氢、氧、氮四种元素组成的,其中氢、氮的原子个数比为28:4=7:1;
(2)帕拉米韦中C、H、N、O元素质量比为(12×15):(1×28):(14×4):(16×4)=45:7:14:16;
(3)每支注射液中帕拉米韦的含量为25mg/支,成人用量为75mg/次,2次/日,则成人每日需注射量为75mg/次×2次=150mg,则每天应注射帕拉米韦注射液150mg÷25mg/支=6支;
故答案为:
(1)4;7:1;
(2)45:7:14:16;
(3)6.
点评:本题难度不大,考查同学们结合标签新信息、灵活运用化学式的有关计算进行分析问题、解决问题的能力.

练习册系列答案
相关题目
根据如图的有关信息判断,下列说法错误的是( )
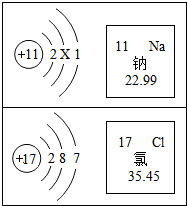

| A、氯元素的核电荷数为17 |
| B、钠的原子结构示意图中X=8 |
| C、钠原子的中子数为11 |
| D、在化学反应中,钠原子容易失去1个电子 |
已知某两种物质在一定条件下能发生化学反应,其反应的微观示意图如图,则下列说法中正确的是(说明:一种小球代表一种元素的原子)( )
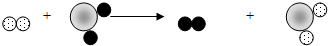

| A、图中的反应物都是化合物 |
| B、该反应属于分解反应 |
| C、该反应不符合质量守恒定律 |
| D、该反应中元素化合价发生了改变 |
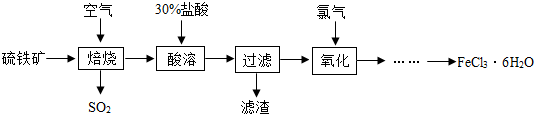
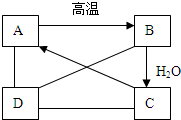 有A、B、C、D四种物质,如图所示,A、B、C在一定条件下可以发生转化,在C溶液中通入CO2,溶液变浑浊,生成白色沉淀A.D与A、B、C均能发生反应,D与A反应有CO2气体产生,D与AgNO3溶液反应,可产生不溶于稀盐酸的白色沉淀.
有A、B、C、D四种物质,如图所示,A、B、C在一定条件下可以发生转化,在C溶液中通入CO2,溶液变浑浊,生成白色沉淀A.D与A、B、C均能发生反应,D与A反应有CO2气体产生,D与AgNO3溶液反应,可产生不溶于稀盐酸的白色沉淀.