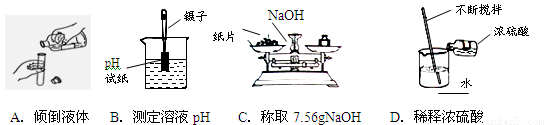
题目内容
(10分)金属在生产和生活中具有广泛的应用。
(1)地壳中含量最高的金属元素是 (写元素符号,下同);人体中含量最高的金属元素是 。
(2)铁制品容易锈蚀,用稀盐酸除铁锈的化学方程式为 。
(3)铁矿石冶炼成铁是一个复杂的过程。把铁矿石、焦炭和石灰石一起加入 ,在高温下,利用其中反应生成的 把铁从铁矿石中还原出来。
(4)炼钢过程中,检验员提取5g钢样,在足量的氧气中充分燃烧,将生成的气体用足量的澄清石灰水充分吸收,得到0.25g白色沉淀。求:①该钢样燃烧时生成二氧化碳的质量;②该钢样中碳的质量分数。
(写出计算过程)
(1)Al Ca ;(2)Fe2O3+6HCl 2FeCl3+3H2O (3)高炉 CO ;(4)①0.11g ②0.6%
【解析】
试题分析:(1)根据地壳中元素的含量可知,地壳中含量最高的金属元素是Al;人体中含量最高的金属元素是Ca (2)铁制品容易锈蚀,用稀盐酸除铁锈的化学方程式为Fe2O3+6HCl 2FeCl3+3H2O; (3)铁矿石冶炼成铁是一个复杂的过程。把铁矿石、焦炭和石灰石一起加入高炉,在高温下,利用其中反应生成的一氧化碳CO;把铁从铁矿石中还原出来。
(4)设生成二氧化碳的质量为x.
CO2+Ca(OH)2=CaCO3↓+H20
100
x 0.25g
44/x=100/0.25g
x=0.11g
0.11g二氧化碳中碳元素的质量=0.11g×12/44×100%=0.03g
钢样中含碳质量分数=0.03/5g× 100%=0.6%
答:钢样中含碳质量分数为0.6%.
考点: 金属、有关化学方程式的计算

 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案下图中容器I、II体积相同,起始时红墨水左右两端液面保持相平,若利用针筒将一定量液体同时注入容器中,并迅速关闭弹簧夹,实验过程中有可能观察到红墨水左低右高的是
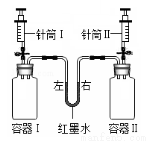
选 项 | 容器I内 | 针筒I内 | 容器II内 | 针筒II内 |
A | 硝酸铵 | 5mL水 | 氢氧化钠 | 5mL水 |
B | 氯化钠 | 5mL水 | 氧化钙 | 5mL水 |
C | 充满二氧化碳 | 5mL氢氧化钠浓溶液 | 充满二氧化碳 | 5mL澄清石灰水 |
D | 0.5g锌粉 | 5g9.8%的稀硫酸 | 0.5g铁粉 | 5g9.8%的稀硫酸 |
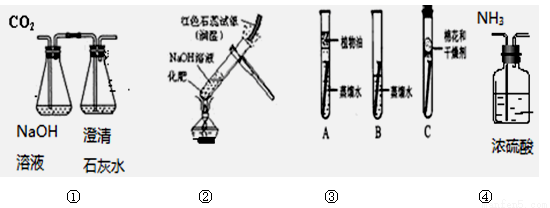
 A.实验①证明CO2能与NaOH溶液反应
A.实验①证明CO2能与NaOH溶液反应