题目内容
18.已知:A是红色粉末,B、C是氧化物,D、I是常见金属,E为胃酸的主要成分,G为单质.它们之间的转化关系如下: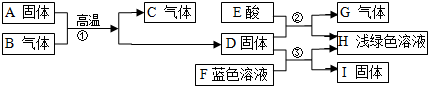
请分析并完成:
(1)气体C的化学式是H2
(2)写出③的化学反应方程式CuCl2+Fe═Cu+FeCl2,该反应的基本类型是置换反应.
(3)②反应前后,溶液的质量B(填序号)
A.不变 B.增大 C.减小.
分析 根据E为胃酸的主要成分,可以知道E为盐酸,而D可以和盐酸反应生成气体和浅绿色溶液,可以知道气体G为氢气,而浅绿色溶液H为氯化亚铁溶液,那么D为铁,进而可以判断出红色粉末A为氧化铁,那么气体B为一氧化碳,而气体C为二氧化碳,固体D可以和蓝色溶液F反应生成氯化亚铁溶液,所以可以判断F为氯化铜溶液,而固体I为铜,至此各物质鉴定完毕,带入验证符合题意,可以据此答题.
解答 解:根据E为胃酸的主要成分,可以知道E为盐酸,而D可以和盐酸反应生成气体和浅绿色溶液,可以知道气体G为氢气,而浅绿色溶液H为氯化亚铁溶液,那么D为铁,进而可以判断出红色粉末A为氧化铁,那么气体B为一氧化碳,而气体C为二氧化碳,固体D可以和蓝色溶液F反应生成氯化亚铁溶液,所以可以判断F为氯化铜溶液,而固体I为铜;带入框图,推断合理;
(1)C是氢气,故填:H2;
(2)反应③为铁和氯化铜溶液的反应,该反应生成了铜和氯化亚铁,其反应的化学方程式为:CuCl2+Fe═Cu+FeCl2;属于置换反应;故填:CuCl2+Fe═Cu+FeCl2;置换;
(3)根据解答可以知道反应②为铁和盐酸的反应,根据它们反应的化学方程式可以知道消耗的铁和生成氢气的质量关系为:
Fe+2HCl═FeCl2+H2↑
56 2
即每消耗56g铁能够生成氢气的质量为2g,所以反应前后溶液的质量要增加,故填:B.
点评 本题为框图式物质推断题,完成此题,可以依据题干提供的信息,找准解题突破口,直接得出有关物质的化学式,然后顺推或逆推得出其他物质的化学式,进而完成解答即可.

练习册系列答案
 孟建平错题本系列答案
孟建平错题本系列答案 超能学典应用题题卡系列答案
超能学典应用题题卡系列答案
相关题目
13.常用燃烧法测定有机物的组成.现取2.3g某有机物在足量的氧气中完全燃烧,生成4.4g CO2和2.7g H2O.对该物质的组成有下列推断:①一定含C、H元素;②一定不含O元素;③可能含O元素;④一定含O元素;⑤分子中C、H、O的元素质量比为12:3:8.其中正确的是( )
| A. | ①② | B. | ①⑤ | C. | ①③⑤ | D. | ①④⑤ |
6.下列实验现象的描述错误的是( )
| A. | 铁丝在氧气中燃烧火星四射 | |
| B. | 铁钉与硫酸铜溶液反应时铁钉表面有红色物质生成 | |
| C. | 镁条在空气中燃烧发出耀眼的强光 | |
| D. | 红磷在氧气中燃烧产生大量浓雾 |
13.菠萝酯(C11H12O3)学名为苯氧乙酸烯丙酯,广泛用于饮料、糖果等食品工业.下列关于菠萝酯化学式的说法正确的是( )
| A. | 菠萝酯由26个原子构成 | B. | 各元素质量的比为11:12:3 | ||
| C. | 菠萝酯的相对分子质量为192 | D. | 氧元素质量分数最小 |
3.如图所示的化学实验基本操作正确的是( )
| A. | 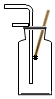 验满 | B. | 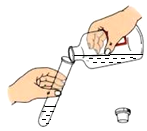 液体取用 | C. | 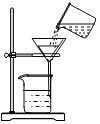 过滤 | D. | 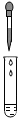 滴加液体 |
10.对于反应M+2N═3P,下列有关叙述正确的是( )
| A. | M、N相对分子质量之和一定等于P的相对分子质量 | |
| B. | 反应前后元素的种类发生了改变 | |
| C. | M、N中若有一种物质为氧化物,则P也一定是氧化物 | |
| D. | 反应前M、N的质量之和一定不小于反应生成的P的质量 |