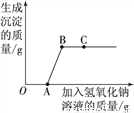
题目内容
几种物质之间的转化关系如图所示,部分产物和反应条件已省去。请回答下列问题:
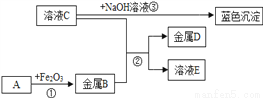
Ⅰ 金属B的活动性________金属D的活动性(填“>”、“<”、“=”);
Ⅱ 若A是一种气体化合物,写出①的化学方程式:____________;
Ⅲ 向C溶液中加入AgNO3溶液,有白色沉淀,加入稀硝酸,沉淀不溶解,写出其化学反应方程式:___________;
Ⅳ 写出溶液C与NaOH溶液反应的基本类型:__________。
> Fe2O3+3CO2Fe+3CO2 ; CuCl2+2AgNO3=Cu(NO3)2+2AgCl↓ ; 复分解反应 【解析】(1)金属B可以置换出金属D,故B的活动性大于D的活动性; (2)氧化铁可以与一氧化碳在高温的条件下反应生成铁和二氧化碳,反应方程式为Fe2O3+3CO2Fe+3CO2; (3)溶液C与氢氧化钠反应生成蓝色的沉淀氢氧化钠,故C溶液是铜盐,溶液C与硝酸银反应...
练习册系列答案
相关题目
化学学习让我们有了很多收获,下列对某一主题的知识归纳,完全正确的一组是
A.物质鉴别 | B.物质除杂 |
硫酸钾和硫酸铵——熟石灰混合研磨、闻气味 羊毛纤维与合成纤维——灼烧、闻气味 鉴别 CaCO3、NaOH、NaCl、NH4NO3 四种固体——加水溶解 | 除去KCl粉末中的少量KClO3——加入二氧化锰,加热除去CO2中的少量CO——将气体缓缓通过灼热的氧化铜 |
C.化学与生活 | D.化学用语中数字的含义 |
①青少年正在长身体,应多吃富含蛋白质的肉类,不吃蔬菜②地沟油经化学方法处理制成航空燃油,实现变废为宝 ③生活中常用的塑料、纤维、合金、玻璃等都是有机合成材料 | ①H2O:一个水分子含有两个氢原子 ②Ca2+:一个钙离子带有两个单位正电荷 ③S2﹣:硫元素的化合价为负二价 |
A. A B. B C. C D. D
A 【解析】A、铵根离子遇到氢氧根离子会有氨气放出,检验羊毛纤维与合成纤维用灼烧、闻气味的方法,CaCO3难溶于水、NaOH溶于水放出热量温度升高,、NaCl溶于水温度不变、NH4NO3溶于水温度降低,故鉴别方法正确; B、除去KCl粉末中的少量KClO3,加入二氧化锰引入了新的杂质,错误; C、人体需要的营养素种类很多,应该全面摄入,不能偏食,错误; D、S2﹣表示的是1...