题目内容
13.小明同学往氢氧化钠溶液中滴加稀盐酸研究中和反应时,忘记了滴加酸碱指示剂.为了确认滴加的盐酸是否已经过量,从烧杯中取少量反应后的溶液于试管中,用某种试剂进行检验.如表是小明同学设计的实验方案,其中错误的是( )| 实验方案 | 使用的试剂 | 判断的方法 |
| A | 铁粉 | 如果有气泡产生,表明盐酸已经过量 |
| B | 氧化铜 | 如果氧化铜溶解,溶液变蓝说明盐酸已经过量 |
| C | 酚酞 | 如果溶液仍为无色,表明盐酸已经过量 |
| D | 碳酸钠粉末 | 如果有气泡产生,表明盐酸已经过量 |
| A. | A | B. | B | C. | C | D. | D |
分析 根据酸的性质来分析实验方案的合理性.
解答 解:A.金属与酸反应生成盐和氢气,所以加入铁粉后,有气泡产生,说明盐酸过量;
B.氧化铜不溶于水,但能溶于酸,所以加入氧化铜,如果能溶解,溶液呈蓝色,说明溶液中含有酸,说明了盐酸过量;
C.酚酞在酸性和中性溶液中都不会变色,所以无法确定溶液是否显酸性;
D.碳酸钠能与盐酸反应生成氯化钠、水和二氧化碳气体,如果有气泡产生,表明盐酸已经过量.
故选C.
点评 解答本题关键是熟悉酸的化学性质,酸能与金属反应、能与金属氧化物反应、能与盐反应、能与酸碱指示剂反应、能与碱反应.

练习册系列答案
 口算题天天练系列答案
口算题天天练系列答案
相关题目
1.如图为水分子分解示意图,下列说法正确的是( )
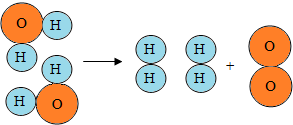

| A. | 水是由两个氢原子和一个氧原子构成 | |
| B. | 一个水分子是由两个氢元素和一个氧元素构成 | |
| C. | 每个氧分子是由2个氧原子构成 | |
| D. | 水分子是由氢元素和氧元素组成的 |
3.下列物质的溶液能使紫色石蕊试液变蓝色的是( )
| A. | 稀盐酸 | B. | 纯碱溶液 | C. | 食盐水 | D. | 食醋 |
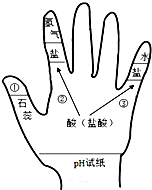 生活中处处有化学,请用所学的化学知识填空.
生活中处处有化学,请用所学的化学知识填空.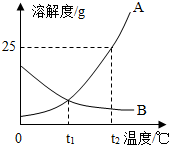 如图为A、B两种固体物质的溶解度曲线.
如图为A、B两种固体物质的溶解度曲线.