题目内容
6.侯德榜是我国著名的化学家,为纯碱和氮肥工业技术的发展作出了杰出的贡献,他发明的侯氏制碱法大大提高了原料的利用率,其工业流程大致如图: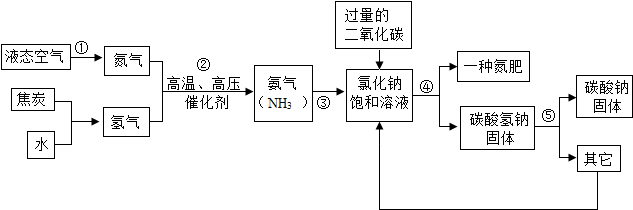
(1)上述流程中,用到的原料有空气、焦炭、水、二氧化碳、氯化钠等.
(2)上述流程中,已知步骤②发生的是化合反应,步骤⑤发生的是分解反应,则步骤②、⑤发生反应的化学方程式是:②N2+3H2$\frac{\underline{\;\;催化剂\;\;}}{高温高压}$2NH3,⑤2NaHCO3$\frac{\underline{\;\;△\;\;}}{\;}$Na2CO3+H2O+CO2↑.
(3)上述流程中,可循环利用的物质是二氧化碳.
(4)上述流程中,“一种氮肥”的化学式是NH4Cl.
分析 (1)根据侯氏制碱法的工业流程图,分析所需的原料即可.
(2)已知步骤②发生的是化合反应,即氮气和氢气在高温、高压、催化剂的作用下生成氨气;步骤⑤发生的是分解反应,即碳酸氢钠固体加热生成碳酸钠、水和二氧化碳,写出反应的化学方程式即可.
(3)根据既是反应物,也是生成物的物质,可以循环使用进行分析解答.
(4)根据二氧化碳与氨气、饱和氯化钠溶液反应,生成一种氮肥,进行分析解答.
解答 解:(1)由侯氏制碱法的工业流程图,用到的原料有空气、焦炭、水、二氧化碳、氯化钠等.
(2)已知步骤②发生的是化合反应,即氮气和氢气在高温、高压、催化剂的作用下生成氨气;步骤⑤发生的是分解反应,即碳酸氢钠固体加热生成碳酸钠、水和二氧化碳,反应的化学方程式分别是N2+3H2$\frac{\underline{\;\;催化剂\;\;}}{高温高压}$2NH3、2NaHCO3$\frac{\underline{\;\;△\;\;}}{\;}$Na2CO3+H2O+CO2↑.
(3)既是反应物,也是生成物的物质可以循环使用,由侯氏制碱法的工业流程图,则可循环利用的物质是二氧化碳.
(4)二氧化碳与氨气、饱和氯化钠溶液反应,生成一种氮肥,由质量守恒定律,该氮肥应是氯化铵,其化学式为:NH4Cl.
故答案为:(1)氯化钠;(2)N2+3H2$\frac{\underline{\;\;催化剂\;\;}}{高温高压}$2NH3;2NaHCO3$\frac{\underline{\;\;△\;\;}}{\;}$Na2CO3+H2O+CO2↑;(3)二氧化碳;(4)NH4Cl.
点评 本题难度不大,理解侯氏制碱法的工业流程图,掌握化学方程式的书写方法、质量守恒定律等是正确解答本题的关键.

练习册系列答案
 三新快车金牌周周练系列答案
三新快车金牌周周练系列答案
相关题目
1.现有失去标签的氯化钙、硝酸银、盐酸、碳酸钠4种无色溶液.将它们编号为甲、乙、丙、丁后,两两混合的现象如表所示.根据实验现象判断甲溶液中溶质的化学式是( )
| 实验顺序 | 实验内容 | 实验现象 |
| ① | 甲+乙 | 有气泡生成 |
| ② | 甲+丙 | 有沉淀生成 |
| ③ | 丙+丁 | 有沉淀生成 |
| ④ | 乙+丙 | 没有现象发生 |
| A. | HCl | B. | CaCl2 | C. | Na2CO3 | D. | AgNO3 |
18.下列微粒结构示意图中,表示阴离子的是( )
| A. | 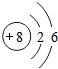 | B. | 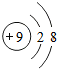 | C. | 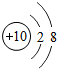 | D. | 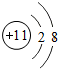 |
15.夏天的傍晩,小明和爸爸妈妈去散步前总喜欢往身上喷点花露水,蚊子闻到花露水的气味就不敢靠近他们了,这一现象说明( )
| A. | 分子之间有间隙 | B. | 分子在不断运动 | C. | 分子由原子构成 | D. | 分子的质量较大 |
16.下列常见的生活物品中所含的主要材料,属于有机合成材料的是( )
| A. | 不锈钢菜刀 | B. | 桑蚕丝围巾 | C. | 橡胶手套 | D. | 玻璃水杯 |
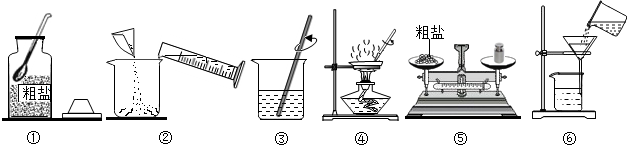
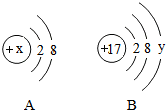 (1)化学用语是学习化学的基本工具,请用化学符号填空:
(1)化学用语是学习化学的基本工具,请用化学符号填空: