题目内容
16. 如图是“XXX”钙片商品标签图.根据标签信息完成下列题.
如图是“XXX”钙片商品标签图.根据标签信息完成下列题.(1)主要成分碳酸钙的相对分子质量为100;
(2)4片中至少含碳酸钙的质量为4.96g.
(3)小蓉同学取出4片片剂,研碎后放入烧杯中,逐滴加入稀盐酸,至不再放出气体为止,共用去10%的稀盐酸146g.求这4片钙片与盐酸反应能生成二氧化碳多少克?(注:请仔细阅读说明书)
分析 根据物质的化学式可以计算物质的相对分子质量;
根据提供的数据可以进行相关方面的计算.
解答 解:(1)CaCO3的相对分子质量为:40+12+16×3=100,
故填:100.
(2)4片中至少含碳酸钙的质量为:1.24g×4=4.96g,
故填:4.96.
(3)设生成二氧化碳的质量为x,
CaCO3+2HCl═CaCl2+H2O+CO2↑,
73 44
146g×10% x
$\frac{73}{146g×10%}$=$\frac{44}{x}$,
x=8.8g,
答:这4片钙片与盐酸反应能生成8.8g二氧化碳.
点评 因为碳酸钙的质量不能确定,因此计算生成的二氧化碳质量时,应该根据稀盐酸的质量减小计算,要注意理解.

练习册系列答案
 星级口算天天练系列答案
星级口算天天练系列答案 芒果教辅达标测试卷系列答案
芒果教辅达标测试卷系列答案
相关题目
11.下表是Ca(OH)2和NaOH的溶解度数据.请回答下列问题:
(1)要想把一瓶接近饱和的Ca(OH)2溶液变成饱和溶液,可采取的方法有加入氢氧化钙(或升高温度)(写出一种即可)
(2)20℃时,191g 饱和NaOH溶液,蒸发10g水后,再降温到20℃,可析出NaOH晶体的质量为19.1g.
(3)现有60℃时含Ca(OH)2和NaOH两种溶质的饱和溶液,若要得到较纯净的NaOH晶体,应采取的物理方法是降温结晶,过滤.
| 温度/℃ | 0 | 20 | 40 | 60 | 80 | 100 | |
| 溶解度/g | Ca(OH)2 | 0.19 | 0.17 | 0.14 | 0.12 | 0.09 | 0.08 |
| NaOH | 31 | 91 | 111 | 129 | 313 | 336 | |
(2)20℃时,191g 饱和NaOH溶液,蒸发10g水后,再降温到20℃,可析出NaOH晶体的质量为19.1g.
(3)现有60℃时含Ca(OH)2和NaOH两种溶质的饱和溶液,若要得到较纯净的NaOH晶体,应采取的物理方法是降温结晶,过滤.
4.下列化学实验基本操作错误的是( )
| A. | 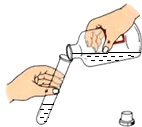 倾倒液体试剂 | B. | 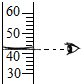 量取一定体积的液体 | ||
| C. | 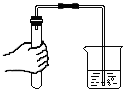 检查装置气密性 | D. | 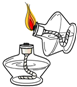 点燃酒精灯 |
5.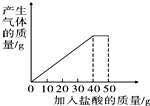 石灰石样品的主要成分是CaCO3(已知其他杂质不与盐酸反应).课外小组同学将50g盐酸分5次加入到20g该石灰石样品中,得到如下部分数据和图象:
石灰石样品的主要成分是CaCO3(已知其他杂质不与盐酸反应).课外小组同学将50g盐酸分5次加入到20g该石灰石样品中,得到如下部分数据和图象:
请计算:
(1)石灰石样品中杂质的质量为4g;
(2)所加盐酸的溶质质量分数.
(3)当加入稀盐酸质量为40克时,所得溶液的质量为48.96克.
 石灰石样品的主要成分是CaCO3(已知其他杂质不与盐酸反应).课外小组同学将50g盐酸分5次加入到20g该石灰石样品中,得到如下部分数据和图象:
石灰石样品的主要成分是CaCO3(已知其他杂质不与盐酸反应).课外小组同学将50g盐酸分5次加入到20g该石灰石样品中,得到如下部分数据和图象:| 次数 | 第1次 | 第2次 | 第3次 |
| 加入盐酸的质量/g | 10 | 10 | 10 |
| 剩余固体的质量/g | 16 | 12 | 8 |
(1)石灰石样品中杂质的质量为4g;
(2)所加盐酸的溶质质量分数.
(3)当加入稀盐酸质量为40克时,所得溶液的质量为48.96克.
 某同学家的下水管道堵塞了,于是他买了一瓶“管道疏通剂”(部分说明如图).疏通剂是利用铝与氢氧化钠溶液反应时放出大量的热,以加快氢氧化钠与毛发等淤积物的作用,反应的原理为:2Al+2NaOH+2H2O=2NaAlO2+3H2↑.使用一包该疏通剂,当铝与氢氧化钠溶液反应后,溶液中剩余氢氧化钠的质量是120克,请说明剩余氢氧化钠的用途和原理:中和酸性废水,NaOH+HCl=NaCl+H2O.
某同学家的下水管道堵塞了,于是他买了一瓶“管道疏通剂”(部分说明如图).疏通剂是利用铝与氢氧化钠溶液反应时放出大量的热,以加快氢氧化钠与毛发等淤积物的作用,反应的原理为:2Al+2NaOH+2H2O=2NaAlO2+3H2↑.使用一包该疏通剂,当铝与氢氧化钠溶液反应后,溶液中剩余氢氧化钠的质量是120克,请说明剩余氢氧化钠的用途和原理:中和酸性废水,NaOH+HCl=NaCl+H2O. 化学与生活息息相关,可以帮助人类认识、改造世界.
化学与生活息息相关,可以帮助人类认识、改造世界.