题目内容
17.有一包白色粉末,可能含有硫酸钡、碳酸钠、氯化钙、氯化钠、硝酸铵中的部分或全部,为确定其组成,设计如下方案:
请回答下列问题:
(1)操作Ⅰ的名称是过滤,需要使用的玻璃仪器有玻璃棒、烧杯和漏斗;
(2)往固体A滴加过量稀硝酸,固体全部溶解,则固体A的化学式为CaCO3;
(3)气体A有刺激性气味,则产生气体A的化学方程式为NH4NO3+NaOH=NaNO3+H2O+NH3↑;
(4)气体B无色无味,则产生该气体的化学方程式为Na2CO3+2HCl=2NaCl+CO2↑+H2O;
(5)通过上述实验,还不能确定的物质的化学式NaCl.
分析 根据加入氢氧化钠溶液后产生气体A,而氢氧化钠能与硝酸铵反应产生氨气,所以气体A是氨气,说明溶液A中含有硝酸铵;溶液B和盐酸能反应产生气体B,而碳酸钠能与盐酸反应产生二氧化碳气体,所以气体B是二氧化碳;碳酸钠能与盐酸反应生成氯化钠、水和二氧化碳,所以溶液C中含有氯化钠;由于固体中含有碳酸钠,且固体加水溶解时产生了固体A,所以固体A是碳酸钠和氯化钙反应生成的碳酸钙和氯化钠,往固体A滴加过量稀硝酸,固体全部溶解,所以A中不含硫酸钡等知识进行分析.
解答 解:加入氢氧化钠溶液后产生气体A,而氢氧化钠能与硝酸铵反应产生氨气,所以气体A是氨气,说明溶液A中含有硝酸铵;溶液B和盐酸能反应产生气体B,而碳酸钠能与盐酸反应产生二氧化碳气体,所以气体B是二氧化碳;碳酸钠能与盐酸反应生成氯化钠、水和二氧化碳,所以溶液C中含有氯化钠;由于固体中含有碳酸钠,且固体加水溶解时产生了固体A,所以固体A是碳酸钠和氯化钙反应生成的碳酸钙和氯化钠,往固体A滴加过量稀硝酸,固体全部溶解,所以A中不含硫酸钡,整个推断过程中不涉及到氯化钠的检验,故可能含有,也可能不含有,所以
(1)经过操作Ⅰ,得到了溶液和固体,属于固液分离,是过滤操作,进行过滤操作时用到的玻璃仪器有玻璃棒、烧杯和漏斗;
(2)碳酸钙和盐酸反应会生成二氧化碳气体,所以固体A的化学式为:CaCO3;
(3)气体A有刺激性气味,则产生气体A的反应是氢氧化钠和硝酸铵反应生成硝酸钠、水和氨气,化学方程式为:NH4NO3+NaOH=NaNO3+H2O+NH3↑;
(4)气体B是二氧化碳,碳酸钠能与盐酸反应生成氯化钠、水和二氧化碳,化学方程式为:Na2CO3+2HCl═2NaCl+H2O+CO2↑;
(5)通过推导可知,还不能确定的物质的化学式NaCl.
故答案为:(1)过滤,漏斗;
(2)CaCO3;
(3)NH4NO3+NaOH=NaNO3+H2O+NH3↑;
(4)Na2CO3+2HCl═2NaCl+H2O+CO2↑;
(5)NaCl.
点评 解答此类题目往往要从物质的颜色、物质之间相互作用时的实验现象等方面进行分析、判断,从而得出正确的结论.

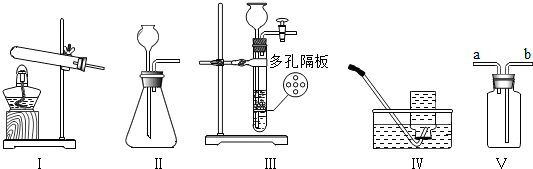
下列有关说法不正确的是( )
| A. | 实验室制取CO2或O2可选用Ⅱ、Ⅳ装置 | |
| B. | 实验室用锌粒和稀硫酸制取H2可选用Ⅱ、Ⅳ装置 | |
| C. | 用氯酸钾制取干燥的氧气可选用Ⅰ、Ⅴ装置,且氧气从b端进入 | |
| D. | 装置Ⅲ与Ⅱ相比,其优点是能控制反应的速率 |
| A. | 干冰升华 | B. | 活性炭吸附冰箱异味 | ||
| C. | 轮胎爆炸 | D. | 燃放烟花 |
| 事 实 | 解 释 | |
| A | 温度计中的水银(汞)热胀冷缩 | 原子大小发生改变 |
| B | 酒香不怕巷子深 | 分子不断运动 |
| C | CO有毒 CO2无毒 | 两种物质的分子构成不同 |
| D | CuSO4溶液和Na2SO4溶液的颜色不同 | 两种溶液中的阳离子不同 |
| A. | A | B. | B | C. | C | D. | D |
| A. | 汽油挥发 | B. | 尘土飞扬 | C. | 酒精燃烧 | D. | 冰雪融化 |
| 物 质 | 甲 | 乙 | 丙 | 丁 |
| 反应前质量(g) | 2 | 4 | 18 | 1 |
| 反应后质量(g) | 8 | X | 8 | 1 |
| A. | 表中X的数值是8 | B. | 丁可能是催化剂 | ||
| C. | 该反应是分解反应 | D. | 该反应中甲和丙的质量之比2:5 |
| A. | 五氧化二磷:O5P2 | B. | 钙离子:Ca+2 | C. | 氯化铝:AlCl | D. | 2个镁原子:2Mg |