题目内容
9.硝酸钾与氯化钾的溶解度曲线如图所示,下列说法正确的是( )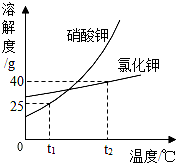
| A. | 从含有少量KCl的硝酸钾溶液中提纯KNO3应采取蒸发结晶法 | |
| B. | t2℃时,向100g水中加入50g氯化钾,充分溶解后,溶液的质量分数为33.3% | |
| C. | t2℃时,两物质的饱和溶液降温至t1℃,析出固体质量较多的是硝酸钾溶液 | |
| D. | 欲配制溶质的质量分数为20%的硝酸钾溶液,温度应不低于t1℃ |
分析 A、硝酸钾的溶解度随温度升高而变化较大,氯化钾的溶解度随温度升高变化不大,所以从含有少量KCl的硝酸钾溶液中提纯KNO3应采取降温结晶法;
B、t2℃时氯化钾的溶解度是40g,据此分析解答;
C、不知饱和溶液的质量,无法判断析出晶体质量多少;
D、饱和溶液中溶质的质量分数=$\frac{溶解度}{溶解度+100g}$×100%,并结合硝酸钾的溶解度分析解答.
解答 解:A、硝酸钾的溶解度随温度升高而变化较大,氯化钾的溶解度随温度升高变化不大,所以从含有少量KCl的硝酸钾溶液中提纯KNO3应采取降温结晶法,故错误;
B、t2℃时氯化钾的溶解度是40g,即100g水中最多溶解40g,所以t2℃时,向100g水中加入50g氯化钾,不能全部溶解,则溶液的质量分数为$\frac{40g}{140g}$×100%<33.3%,故错误;
C、不知饱和溶液的质量,无法判断析出晶体质量多少,故错误;
D、饱和溶液中溶质的质量分数=$\frac{溶解度}{溶解度+100g}$×100%,设形成20%的硝酸钾饱和溶液时硝酸钾的溶解度是x,则有$\frac{x}{100g+x}$×100%=20%,解得x=25g,恰好是t1℃时硝酸钾的溶解度,则温度不低于t1℃,正确;
故选:D.
点评 了解溶解度曲线意义、饱和溶液中溶质的质量分数和溶解度之间的关系,等质量的饱和溶液降低相同的温度溶解度变化大的析出晶体多等知识,才能结合题意灵活分析解答问题.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
17.下列图象能正确反映其对应关系的是( )
| A. |  某温度下,向一定量接近饱和的硝酸钾溶液中不断加入过量的硝酸钾晶体 | |
| B. | 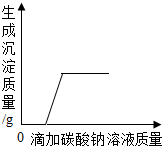 向一定量的稀盐酸和氯化钙的混合溶液中不断滴入碳酸钠溶液至过量 | |
| C. | 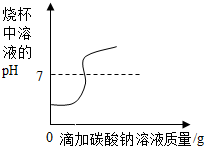 向氢氧化钠溶液中滴加过量的稀盐酸 | |
| D. | 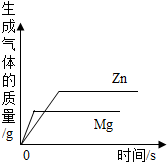 等质量的镁和锌同时分别放入两份溶质质量分数相同的足量稀盐酸中 |
14. 通过做对照实验得出正确的结论是实验探究的重要方法.利用如图所示实验回答问题:
通过做对照实验得出正确的结论是实验探究的重要方法.利用如图所示实验回答问题:
(1)通过图中对比探究,可知铁的锈蚀与哪些因素有关?
(2)本实验共有2组对照组.任选一组,写出其目的和现象分别是什么?
 通过做对照实验得出正确的结论是实验探究的重要方法.利用如图所示实验回答问题:
通过做对照实验得出正确的结论是实验探究的重要方法.利用如图所示实验回答问题:(1)通过图中对比探究,可知铁的锈蚀与哪些因素有关?
(2)本实验共有2组对照组.任选一组,写出其目的和现象分别是什么?
1.除去下列各物质中混有的少量杂质(括号内为杂质),下列选项中所用试剂正确的是( )
| A. | 铁粉(氧化铁):稀硫酸 | B. | 二氧化碳(氯化氢):氢氧化钠溶液 | ||
| C. | 氯化钠溶液(硫酸钠):硝酸钡溶液 | D. | 氯化钙溶液(盐酸):碳酸钙粉末 |
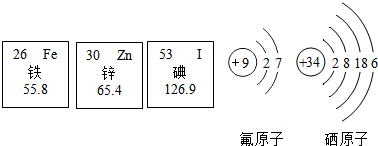 人体中必需的微量元素铁、氟、锌、硒、碘等,虽然含量少,但对健康至关重要.如图提供几种微量元素的相关信息,请认真分析并回答下列问题:
人体中必需的微量元素铁、氟、锌、硒、碘等,虽然含量少,但对健康至关重要.如图提供几种微量元素的相关信息,请认真分析并回答下列问题: