题目内容
14.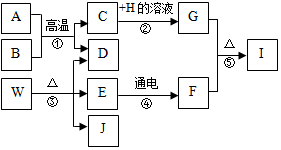 以下物质为初中化学常见物质,它们存在如图所示的转化关系.已知A为铁锈的主要成分,W绿色固体,H的溶液呈蓝色,常温下B、D、F均为无色气体且BD元素组成完全相同.(反应②、④的个别生成物已略去)
以下物质为初中化学常见物质,它们存在如图所示的转化关系.已知A为铁锈的主要成分,W绿色固体,H的溶液呈蓝色,常温下B、D、F均为无色气体且BD元素组成完全相同.(反应②、④的个别生成物已略去)(1)写出化学式:DCO2,JCuO;
(2)写出反应①③④的化学方程式:
①Fe2O3+3CO$\frac{\underline{\;高温\;}}{\;}$2Fe+3CO2
③Cu2(OH)2CO3$\frac{\underline{\;\;△\;\;}}{\;}$2CuO+CO2↑+H2O
④2H2O$\frac{\underline{\;通电\;}}{\;}$2H2↑+O2↑.
分析 本题的突破口有以下几处:由A为铁锈的主要成分可知A为Fe2O3;W绿色固体,能加热分解生成三种物质,由E在常温下为无色液体,结合转化关系框图E在通电条件下生成气体F,可猜想E为水H2O,故W是碱式碳酸铜;生成的D和J是氧化铜和二氧化碳中的一种,D是无色气体,故D是二氧化碳,J是氧化铜;B和D的组成元素相同,故B是一氧化碳,一氧化碳能与氧化铁高温反应生成铁和二氧化碳,故C是铁;由H的溶液呈蓝色,可猜想H为可溶性铜盐,常见的为硫酸铜CuSO4;铁能与硫酸铜反应生成硫酸亚铁和铜,铜能与F加热反应生成J,故F是氧气,J是氧化铜,据此解答.
解答 解:由A为铁锈的主要成分可知A为Fe2O3;W绿色固体,能加热分解生成三种物质,由E在常温下为无色液体,结合转化关系框图E在通电条件下生成气体F,可猜想E为水H2O,故W是碱式碳酸铜;生成的D和J是氧化铜和二氧化碳中的一种,D是无色气体,故D是二氧化碳,J是氧化铜;B和D的组成元素相同,故B是一氧化碳,一氧化碳能与氧化铁高温反应生成铁和二氧化碳,故C是铁;由H的溶液呈蓝色,可猜想H为可溶性铜盐,常见的为硫酸铜CuSO4;铁能与硫酸铜反应生成硫酸亚铁和铜,铜能与F加热反应生成J,故F是氧气,J是氧化铜,带入框图,推断合理;
(1)D是二氧化碳,J是氧化铜,故填:CO2;CuO;
(2)一氧化碳与氧化铁高温反应生成铁和二氧化碳,故填:Fe2O3+3CO$\frac{\underline{\;高温\;}}{\;}$2Fe+3CO2;
(3)碱式碳酸铜受热分解生成氧化铜、水和二氧化碳,故填:Cu2(OH)2CO3$\frac{\underline{\;\;△\;\;}}{\;}$2CuO+CO2↑+H2O;
(4)水通电分解生成氢气和氧气,故填:2H2O$\frac{\underline{\;通电\;}}{\;}$2H2↑+O2↑.
点评 根据物质的颜色、状态、气味等重要性质及主要成分的分析,找出特殊物质,形成对推断的突破,然后利用转化关系等进行合理地推断,从而梳理出解决问题的思路.

 名牌中学课时作业系列答案
名牌中学课时作业系列答案 明天教育课时特训系列答案
明天教育课时特训系列答案 浙江新课程三维目标测评课时特训系列答案
浙江新课程三维目标测评课时特训系列答案 周周清检测系列答案
周周清检测系列答案| A. | 节约用水和防治水体污染是爱护水资源的有效途径 | |
| B. | 自来水厂净水过程中所采用的方法包括:沉淀、吸附、蒸馏 | |
| C. | 水是由氢气和氧气组成的混合物 | |
| D. | 长期饮用纯净水有益身体健康 |
| A. | O2 | B. | MnO2 | C. | KClO3 | D. | C2H5OH |




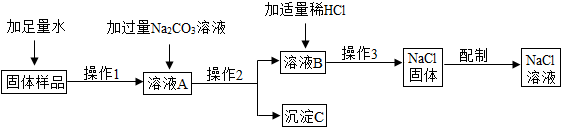 请据图回答:
请据图回答: