题目内容
6.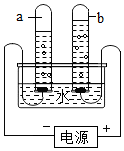 实验是化学学习的一种重要手段,如利用电解水实验可探究水的组成.请根据电解水实验回答下列问题:通电后电极上出现气泡,并汇集到试管上端.负极产生的气体与正极产生的气体的体积比为2:1,经检验,负极产生的气体是H2(填化学式),正极产生的气体是O2(填化学式).从而证明了水是氢元素和氧元素组成的,写出电解水的化学反应文字表达式水$\stackrel{通电}{→}$氢气+氧气.
实验是化学学习的一种重要手段,如利用电解水实验可探究水的组成.请根据电解水实验回答下列问题:通电后电极上出现气泡,并汇集到试管上端.负极产生的气体与正极产生的气体的体积比为2:1,经检验,负极产生的气体是H2(填化学式),正极产生的气体是O2(填化学式).从而证明了水是氢元素和氧元素组成的,写出电解水的化学反应文字表达式水$\stackrel{通电}{→}$氢气+氧气.
分析 根据电解时实验观察到试管中气体的体积a中多,则a中为氢气,b中为氧气,且体积比为2:1,氢气在与电源正极相连的一端的试管中生成,则可判断电源的正负极,再利用氢气和氧气的性质来分析解答.
解答 解:通电后电极上出现现象为气泡,并汇集到试管上端,正极产生的气体能支持燃烧,则正极产生的气体是氧气,负极产生的气体能燃烧、产生淡蓝色的火焰.负极产生的气体是氢气.正极产生的气体是氧气,化学式为:O2;负极是氢气,化学式为:H2,体积比为1:2,所以负极上产生的气体与正极上产生的气体的体积比为2:1.从而证明了水是氢元素和氧元素组成的,电解水的化学反应文字表达式为:水$\stackrel{通电}{→}$氢气+氧气;
故答案为:气泡;2:1;H2,O2;氢元素和氧元素;水$\stackrel{通电}{→}$氢气+氧气;
点评 熟练掌握水电解实验的原理、现象、结论是解答本题关键,要熟记正氧负氢,氢二氧一的含义.

练习册系列答案
 冲刺100分1号卷系列答案
冲刺100分1号卷系列答案
相关题目
17.下列材料属于天然材料的是( )
| A. | 羊毛 | B. | 钢铁 | C. | 玻璃 | D. | 食品保鲜膜 |
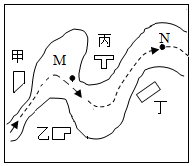 某中学环保监测小组的同学在一条鱼虾绝迹的小河边发现四所工厂,如图.这些工厂向小河所排放的废水中各含一种化合物,经检测发现:①甲处河水呈黄色;②乙处河水呈红褐色浑浊状;③丙处河水变澄清;④丁处河水不断冒气泡;⑤M处水样PH>7,加足量HNO3再加BaCl2溶液后无沉淀;⑥N处水样PH<7.?
某中学环保监测小组的同学在一条鱼虾绝迹的小河边发现四所工厂,如图.这些工厂向小河所排放的废水中各含一种化合物,经检测发现:①甲处河水呈黄色;②乙处河水呈红褐色浑浊状;③丙处河水变澄清;④丁处河水不断冒气泡;⑤M处水样PH>7,加足量HNO3再加BaCl2溶液后无沉淀;⑥N处水样PH<7.?
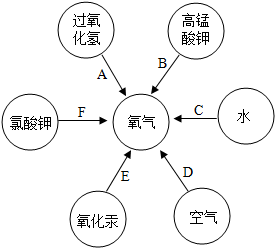 经过一段时间的学习,我们学过了六种途径可以制氧气,如图所示.
经过一段时间的学习,我们学过了六种途径可以制氧气,如图所示.